ニュース&トピックス 稀少疾患である「手足が動きにくくなる末梢神経変性病」の創薬標的分子および創薬候補を解明!|プレスリリース
- 生命科学部
- 分子生命科学科
- 研究活動
2022.05.10
プレスリリース
稀少疾患である「手足が動きにくくなる末梢神経変性病」の創薬標的分子および創薬候補を解明! -- ドラッグリポジショニングによる稀少神経疾患の新たなる治療戦略|プレスリリース
ポイント
- 研究の背景
- 神経システムは中枢神経系(central nervous system)と末梢神経系(peripheral nervous system)に大別される。前者は主に脳や脊髄から構成され、後者は四肢(手足)まで複雑にネットワークが形成されている感覚神経などがある。脳や脊髄の神経疾患は進行が早い場合は致死性であることが多く、その治療は緊急を要する。そのため治療方法の確立を求められることが多い。一方、末梢神経障害はほとんどの場合、生命への直接的な影響は大きくはないとされ、その治療方法の確立に関する研究が遅れることがある。しかしながら、クオリティ・オブ・ライフ(QOL)の観点からも末梢神経障害の研究の重要性は中枢神経系の研究の重要性と遜色はないと考えられる。
当該研究は、遺伝的要因で発症するシャルコーマリーツース病(Charcot-Marie-Tooth disease; CMT病)を対象とする。CMT病は先天性の末梢神経変性疾患であり、特異的な治療薬がない病気である。とくにグリア細胞の病態を主たる原因とする疾患をCMT1とよび、神経細胞の病態を主たる原因とする疾患をCMT2とよぶ。CMT病全体での病因を有する頻度は2500から3000人に1人である。これは国内外を通じても同じ頻度である。 - 成果について
- 2W型CMT病(CMT2W)の責任遺伝子であるHARS1の変異が原因でおこる末梢神経(感覚神経)変性疾患の細胞モデルを先駆けて作成し、その細胞病態の原因が細胞内凝集体(アグリソーム)の形成にあることを突きとめた。HARS1とよばれるタンパク質に異常が生じると、それがアグリソームの形成を誘導し、感覚神経細胞の分化や発生に異常をもたらすと考えられた。一方、これらの異常は抗てんかん薬のひとつであるバルプロ酸で改善できることを明らかにした。バルプロ酸の作用機序(Mechanism of action; MOA)としては神経分化に重要な細胞内リン酸化経路(JNK経路)が関与していることを明らかにし、バルプロ酸(デパケンという名が一般名)がそれを促進することによることも併せて明らかにした。
- 今後の展望
- 研究成果が細胞モデルの結果を中心としているため、これらが当研究室で独自に開発した感覚神経の共培養システムによる人工感覚神経組織でも、この病態を再現できるか検討しなければならない。また、マウスモデルにおいても再現できるか明らかにすべきである。その過程において前臨床試験を行い、バルプロ酸を用いて治療効果が期待できるか検討したい。
概要
- 新たに見つかった疾患原因とその細胞での治療効果
- HARS1とよばれるタンパク質はタンパク質翻訳システムの中核をなす分子にひとつである。先行研究においては、このタンパク質が未成熟の状態(壊れやすい状態)でできあがるため、タンパク質翻訳システムが機能異常に陥り、感覚神経の異常につながると考えられていた。
今回、この壊れやすい状態でできあがるHARS1がアグリソームに蓄積し、そのストレス応答を誘導することで、感覚神経の変性疾患の細胞病態(分化阻害など)がおこることを明らかにした。重要なことは、バルプロ酸によるJNK経路を活性化することで、細胞病態の多くの異常が改善できることを明らかにした点である。
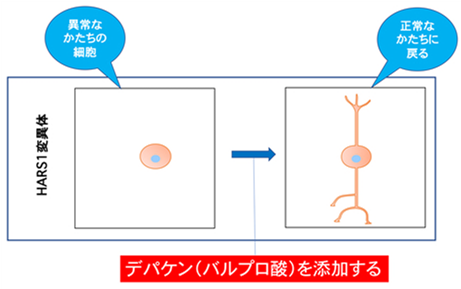 図1 HARS1変異で誘導される異常タンパク質が原因で、神経分化が阻害される。 この病態細胞にバルプロ酸を添加すると神経分化が誘導される。
図1 HARS1変異で誘導される異常タンパク質が原因で、神経分化が阻害される。 この病態細胞にバルプロ酸を添加すると神経分化が誘導される。
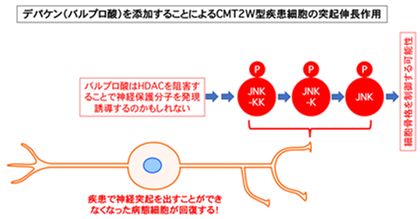 図2 バルプロ酸で神経分化が誘導されるメカニズム(Mechanism of action; MOA)のひとつとして細胞内リン酸化経路(JNK経路)を活性化することがあげられる。
図2 バルプロ酸で神経分化が誘導されるメカニズム(Mechanism of action; MOA)のひとつとして細胞内リン酸化経路(JNK経路)を活性化することがあげられる。
これらの研究は2021年度まで在学の東京薬科大学生命科学部分子神経科学研究室の博士前期課程(修士課程)2年の目々澤史織らを中心にして行われた研究成果です。
原著論文
- 科学誌名
- 国際神経化学誌(Neurochemical Research)に掲載される (The ISN-APSN meeting (Kyoto) special issue [国際学会特集号])
- 論文題名
- The antiepileptic valproic acid ameliorates Charcot-Marie-Tooth 2W (CMT2W) disease-associated HARS1 mutation-induced inhibition of neuronal cell morphological differentiation through c-Jun N-terminal kinase
- 著者氏名
- Shiori Memezawa(目々澤史織、筆頭著者), Takanari Sato, Arisa Ochiai, Miku Fukawa, Sui Sawaguchi, Kazunori Sango, Yuki Miyamoto, and Junji Yamauchi(山内淳司 [*]、責任著者)
- 所属[*]
- 東京薬科大学生命科学部、国立成育医療研究センター薬剤治療研究部(兼任)、東京都医学総合研究所糖尿病研究プロジェクト(兼任)
- 論文情報
- Doi
- 10.1007/s11064-022-03587-z
関連リンク
取材に関するお問い合わせ先
- 東京薬科大学 総務部 広報課
-
- 042-676-6711(8:45~17:00 月~金、祝日は除く)
- お問い合わせフォーム
研究に関するお問い合わせ先
- 東京薬科大学 生命科学部 分子神経科学研究室 教授 山内淳司
-
- 042-676-7164
- yamauchi@toyaku.ac.jp









