ニュース&トピックス 完全ヒト抗体産生マウスを用いた迅速な創薬プラットフォームの構築に成功~最短60日で感染症抗体を作製、今後のパンデミックへの「備え」に期待~|プレスリリース
- 生命科学部
- プレスリリース
- その他
- 応用生命科学科
- 研究活動
2025.10.21

ポイント
- ① 完全ヒト抗体産生(TC-mAb)マウス、② 迅速な免疫法、③ シングルB細胞解析技術、もしくは哺乳類細胞ディスプレイシステムを基盤とする、迅速なヒト抗体医薬品候補の取得を可能とする創薬プラットフォーム「Express Hu-mAb System」の構築に成功しました。
- 完全ヒト抗体産生(TC-mAb)マウスを対象とし、30日間で力価や抗体価が急上昇する迅速な免疫法を確立しました。SARS-CoV-2オミクロン株に中和活性を示すマウスからIgG+ B細胞を回収し、シングルBセル解析から得た情報を活用して、抗体作製を行い、武漢株とオミクロンBA.5株を中和できる広域中和抗体の作製を30日間で成功しました(合計60日間)。
- SARS-CoV-2オミクロン株を中和しなかったマウスの免疫組織を用いて、哺乳類細胞ディスプレイシステムによる抗体遺伝子cDNAライブラリーの作製・スクリーニング法を確立し、武漢株とオミクロンBA.5株の両方を中和できる広域中和抗体の作製を60日間で成功しました(合計90日間)。
- 「Express Hu-mAb System」は、新型コロナウイルス感染症以外にも応用できることから、今後のパンデミックの脅威に対する「備え」として期待されています。
概要
鳥取大学染色体工学研究センターの濱道 修生 特命助教、香月 康宏 教授、東京薬科大学の宇野 愛海 助教、冨塚 一磨 教授らの共同研究グループは、ウイルス感染症対策の一環として、迅速にヒト抗体医薬品注1)を創出できる創薬プラットフォーム注2)「Express Hu-mAb System」の構築に成功しました。
世界的に大流行した新型コロナウイルス感染症注3)は、創薬分野において数多くの課題を浮き彫りにしました。その一つが、SARS-CoV-2ウイルス注4)の変異が短期間に起こるため、ヒト抗体医薬品の開発から生産の期間を5-6ヶ月まで短縮しないと、新規変異株に対応できないという課題です。そこで本研究グループは、スピードに重点を置きつつ、医薬品候補の開発可能性注5)や製造可能性注6)の要素を加味するため、① 完全ヒト抗体産生(TC-mAb)マウス注7)、② 迅速な免疫法注8)の確立と③ シングルB細胞解析技術、もしくは哺乳類細胞ディスプレイシステム注9)を基盤とする新規モノクローナル抗体取得技術の開発を組み合わせ、この課題の解決に取り組みました。本創薬プラットフォームを活用し、SARS-CoV-2武漢株とオミクロンBA.5株を中和する広域中和抗体注10)をシングルB細胞解析技術では合計60日間、哺乳類細胞ディスプレイシステムでは合計90日間での作製に成功しました。「Express Hu-mAb System」は、今後のパンデミックの脅威に対する「備え」として期待されます。本研究は、立教大学の末次 正幸 教授と九州大学の福原 崇介 教授らとの共同研究で行われました。
本研究成果は、2025年10月11日(日本時間)の「Molecular Therapy」誌でオンライン公開されました。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(CREST, LEAP)、生命科学・創薬研究支援基盤事業(BINDS)、科学技術振興機構(JST)の戦略的創造研究推進事業(CREST)、並びに生命創成探究センター(ExCELLS)等からの支援を受けて行われました。
研究の背景と経緯
世界的に大流行した新型コロナウイルス感染症(COVID-19)は社会の様々な領域において影響をもたらしました。創薬分野においても例外でなく、ヒト抗体医薬品開発を含め数多くの課題が浮き彫りになりました。つまり、SARS-CoV-2ウイルスの変異が短期間に起こるため、ヒト抗体医薬品の開発から生産の期間を5-6ヶ月まで短縮しないと、新規変異株に対応できないという課題です。そこで世界各国の研究グループがスピードを重視した創薬プラットフォームの開発を進めるなか、本研究グループは、スピードに重点を置きつつ、抗体医薬品候補の開発可能性や製造可能性の要素を加味した独自の創薬プラットフォーム「Express Hu-mAb System」の構築に成功しました。
研究の内容
本創薬プラットフォーム「Express Hu-mAb System」は、主に3つの内容から成り立っています。① 完全ヒト抗体産生(TC-mAb)マウスを用いることで、キメラ化やヒト化注11)を要しない完全ヒト抗体が作製できます。また、TC-mAbマウスは抗原特異的抗体注12)の産生に有利であることが知られています。② 迅速な免疫法の確立により、従来の数ヶ月を要した免疫期間に対して、30日間で十分な力価や抗体価注13)の上昇が実現されました。③ シングルBセル解析技術、もしくは抗体製造に用いられるChinese hamster ovary (CHO)細胞株注14)を用いた哺乳類細胞ディスプレイシステムを確立し、これらを基盤とした新規モノクローナル抗体取得技術を開発しました。上記3つの特徴の組み合わせから、開発可能性や製造可能性を維持した抗体再設計も期待でき、「3本の矢」のような強力な創薬プラットフォームが構築されました。
本研究では「Express Hu-mAb System」の実用性を検討するため、TC-mAbマウスにSARS-CoV-2武漢株のreceptor binding domain (RBD)注15)、スパイクタンパク質注16)アルファ株、ベータ株とデルタ株を抗原注17)として免疫し、免疫しなかったオミクロン株も中和できる広域中和抗体の作製を試みました。従来の免疫法では抗原を免疫し、この抗原に対する抗体作製が一般的ですが、あえて常識とは異なる免疫を行いました。本研究では30日間で力価や抗体価が急上昇する迅速な免疫法を確立しました。また抗血清の解析から、オミクロン株に中和活性を示すマウスを選別しました。さらに、この個体からIgG+ B細胞注18)を回収し、シングルBセル解析注19)を用いてモノクローナル抗体を取得し、武漢株とオミクロンBA.5株を中和できるクロノタイプ11広域中和抗体の作製を30日間で成功しました。また、オミクロン株を中和しなかったマウス個体の免疫組織を用いて、哺乳類細胞ディスプレイシステムによる再設計された抗体遺伝子cDNAライブラリー注20)の作製・スクリーニング法を確立し、武漢株とオミクロンBA.5株を中和できるM5419S09Ab01広域中和抗体を60日間での作製に成功しました。
今後の展開
COVID-19からの教訓、さらに今後のパンデミック対策において、迅速な対応は極めて重要です。スピード重視の観点から、我々は計60日間で広域中和抗体を作製し、中和抗体cDNAライブラリーから広域中和抗体の再設計を計90日間で成功しました。上記の実験結果は、迅速、高効率且つシンプルな創薬プラットフォームの開発を示すものです。本研究のレパトア解析注21)から、TC-mAbマウスのB細胞がCOVID-19患者の免疫応答を再現していることが分かり、この結果はワクチン開発や評価において、TC-mAbマウスの有用性を示唆するものです。また、哺乳類細胞ディスプレイシステムと既存抗体cDNAライブラリーを用いて機能性抗体の再設計が示され、さらなる抗体医薬品の開発への応用が有望視されます。「Express Hu-mAb System」は、COVID-19以外の感染症にも応用できることから、今後のパンデミックの脅威に対する「備え」として期待されています。
参考図
図1.本研究の概要図
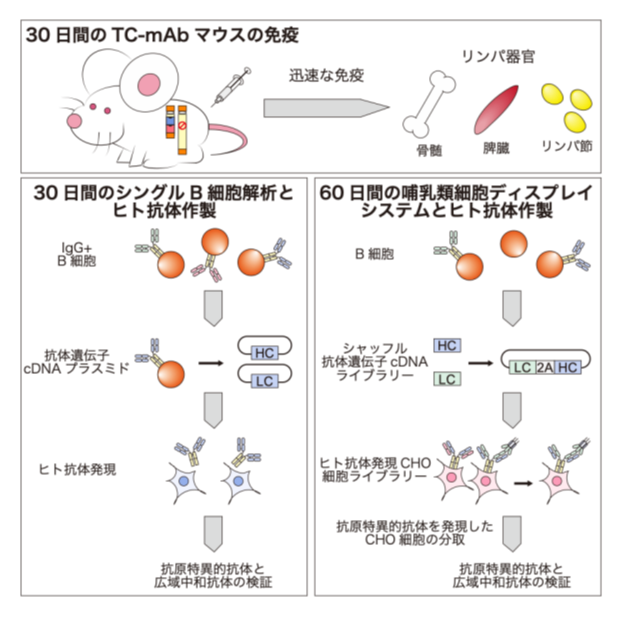
「Express Hu-mAb System」は、① TC-mAbマウス、② 迅速な免疫法と③ シングルBセル解析技術、あるいは哺乳類細胞ディスプレイシステムにより成り立っています。本研究では、TC-mAbマウスの免疫を30日間で完了し、リンパ器官を摘出しました。オミクロン株に中和活性を示すマウスからIgG+ B細胞を回収し、シングルBセル解析から抗体作製を行い、武漢株とオミクロンBA.5株を中和できるクロノタイプ11広域中和抗体の作製を30日間で成功しました。また、オミクロン株を中和しなかったマウスの免疫組織を用いて、哺乳類細胞ディスプレイシステムによる抗体遺伝子cDNAライブラリー)の作製・スクリーニング法を確立し、武漢株とオミクロンBA.5株を中和できるM5419S09Ab01広域中和抗体を60日間で作製しました。
図2.TC-mAbマウスの抗血清と取得モノクローナル抗体の解析
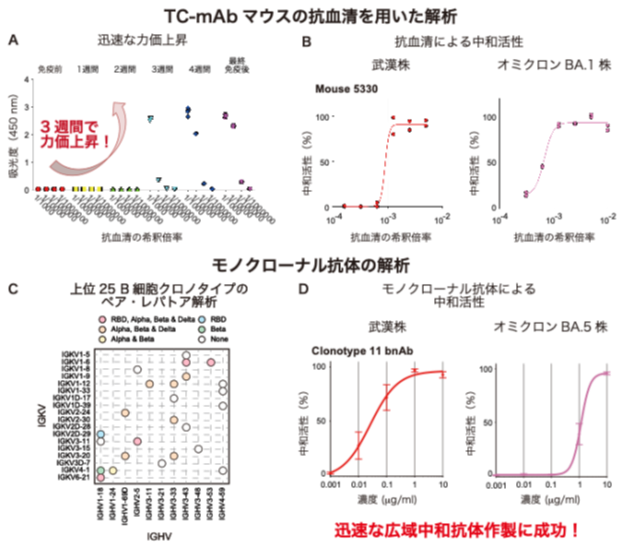
(A) TC-mAbマウスの抗血清を希釈し、武漢株のRBDに対する反応を確認した。免疫開始から3週間後で力価が上昇し、最終免疫後では抗血清を10万倍希釈しても、反応が認められた。(B) TC-mAbマウスの抗血清によるSARS-CoV-2武漢株とオミクロンBA.1株に対する中和活性を示す。(C) シングルB細胞のレパトア解析から使用されたヒト抗体遺伝子が判明された。色は各抗体が結合する抗原を示す。(D) 本研究より作製されたクロノタイプ11広域中和抗体のSARS-CoV-2武漢株とオミクロンBA.5株に対する中和活性を示す。
図3. 哺乳類細胞ディスプレイシステムによる抗体遺伝子cDNAライブラリー構築とスクリーニングの概要
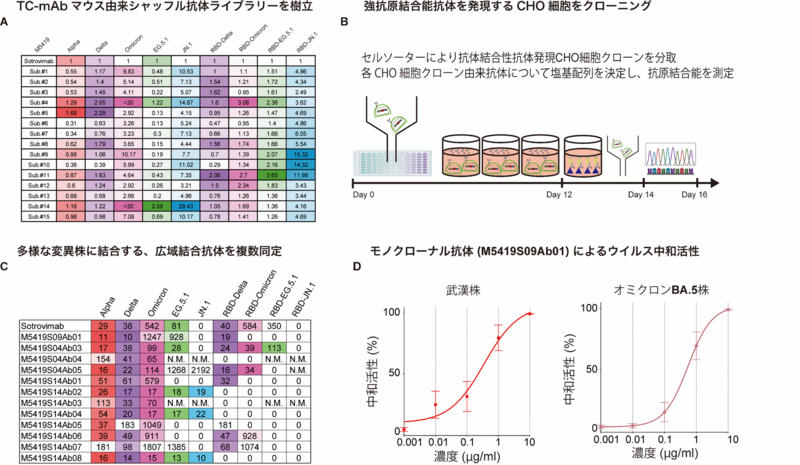 図3.哺乳類細胞ディスプレイシステムによる抗体遺伝子cDNAライブラリー構築とスクリーニングの概要
図3.哺乳類細胞ディスプレイシステムによる抗体遺伝子cDNAライブラリー構築とスクリーニングの概要
(A) 哺乳類細胞ディスプレイシステムを構築するために、まずTC-mAbマウス由来のB細胞から抗体遺伝子をPCR法で増幅し、CHO細胞に導入した。抗体遺伝子は哺乳類細胞ディスプレイ法を用いて15のサブライブラリーに分割、樹立した。培養上清中に分泌された抗体について、各SARS-CoV-2ウイルス変異株タンパク質への結合能を評価し、優れた抗体を含むサブライブラリーを同定した。(B) サブライブラリーを構成するCHO細胞集団から、強い抗原結合能を示す細胞をセルソーターで単離した。単離したCHO細胞クローンが発現する抗体の塩基配列を決定し、各種抗原への結合能を測定することで、広域結合能を示す有望なモノクローナル抗体をスクリーニングした。(C) スクリーニングにより得られたモノクローナル抗体について、抗原結合能(EC50)を算出した。 (D) 哺乳類細胞ディスプレイシステムから得られたモノクローナル抗体(M5419S09Ab01)の広域中和抗体としての活性を、SARS-CoV-2武漢株およびオミクロンBA.5株を用いて評価した。
用語解説
注1)ヒト抗体医薬品:
抗体は、病気の原因となる抗原に対し高い特異性があるため、医薬品として利用されています。ヒト抗体とは、ヒトの基本構造を持つ抗体です。
注2)創薬プラットフォーム:
複数の最先端技術を組み合わせ創薬の効率化と成功率を向上させるシステムである。コロナ禍において、スピードを重視した数多くの創薬プラットフォームが開発されました。
注3)新型コロナウイルス感染症:
新型コロナウイルス感染症は、SARS-CoV-2ウイルスを病原体とする感染症です。2019年12月に中国湖北省武漢市にて原因不明の肺炎の報告(武漢株)から始まり、世界的に大流行しました。全世界の累積感染者数は、778,653,604人であり、累積死亡者数は、7,102,195人になります(世界保健機関、2025年9月14日)
注4)SARS-CoV-2ウイルス:
SARS-CoV-2ウイルスは、新型コロナウイルス感染症の病原体である。2019年12月、中国湖北省武漢市にて初めて発見された以降、迅速な変異を続けパンデミックを起こした。
注5)開発可能性:
抗体を医薬品として開発するためには、タンパク質としての品質管理が必要です。治療に用いる医薬品として製剤化するにあたり、正しい立体構造を形成すること、医薬品溶液中で凝集しにくいこと、特異的に結合すること等が挙げられます。また、哺乳類細胞特有の糖鎖修飾も抗体の性質に影響を及ぼします。本創薬プラットフォームでは、医薬品開発可能性として、上記の重要な抗体の特性をもつ、哺乳類細胞膜状に高密度で安定発現した状態でも機能する抗体を、優先的に取得できると期待されます。
注6)製造可能性:
抗体製造には、抗体産生細胞の作製、抗体産生細胞の培養と抗体の精製の3つのステップがあります。そのため、抗体の大量生産に適した細胞株が樹立できることが重要です。本創薬プラットフォームによる選抜を経た抗体は、抗体産生細胞の生育への悪影響が少なく、抗体製造時の生産性に優れた抗体であると期待されます。
注7)完全ヒト抗体産生(TC-mAb)マウス:
鳥取大学独自の染色体工学技術を用いて作製された完全ヒト抗体を産生するマウスです。内因性マウス抗体遺伝子は破損されているため、マウス抗体は産生されません。
注8)免疫法:
抗体作製において、目的の抗体を産生するため、動物に抗原を投与する方法です。抗原の投与量や投与部位などを最適化し、目的の抗体を作製します。
注9)哺乳類細胞ディスプレイシステム:
抗体や受容体などのタンパク質を哺乳類細胞表面に発現させ、細胞単位で抗原結合能を評価・選別するスクリーニング技術です。CHO細胞などを用いることで、天然に近い立体構造や糖鎖修飾を保持した状態で抗体を提示でき、高親和性抗体や機能改良抗体の取得が可能になります。また、抗体のアミノ酸配列によってはCHO細胞での発現が困難な場合がありますが、このシステムでは、CHO細胞内で安定して発現できる抗体が自然に選抜されるため、開発可能性や製造可能性を維持した抗体の取得が期待されます。
注10)広域中和抗体:
様々な系統のウイルスを中和できる抗体のことを広域中和抗体と呼びます。新型コロナウイルス感染症において、代表的な広域中和抗体は武漢株やオミクロン株を中和するソトロビマブである。
注11)キメラ化やヒト化:
従来のマウスでは、マウス抗体が産生されるため、抗体医薬品として利用するためには、ヒト抗体の構造に近づける必要がありました。そのためマウス抗体の特定部位とヒト抗体の特定部位を組み合わせたキメラ化やヒト化が行われました。完全ヒト抗体では、100%ヒト抗体の構造を持つため、キメラ化やヒト化は不要です。
注12)抗原特異的抗体:
目的とした抗原に対し、特異的に結合する抗体のことを抗原特異的抗体と呼びます。
注13)力価や抗体価:
免疫法を評価する方法である。力価は、抗血清を何倍希釈しても抗原に対する反応が確認できるかを示す数値です。抗体価は、血清中の抗体の濃度を表します。
注14)Chinese hamster ovary (CHO)細胞株:
チャイニーズハムスター卵巣由来の培養細胞株であり、哺乳類タンパク質発現に最も汎用される宿主細胞の一つです。安定した増殖性と高いタンパク質発現能、さらに糖鎖修飾を付与できる特性を有するため、抗体医薬品をはじめとする再組換えタンパク質製造に広く利用されています。
注15)receptor binding domain (RBD):
RBDの日本語訳は「受容体結合ドメイン」である。SARS-CoV-2は、RBDを用いてヒト細胞へ侵入することで知られている。
注16)スパイクタンパク質:
SARS-CoV-2の表面タンパク質であり、スパイクタンパク質の一部は、ヒト細胞への侵入に重要なRBDである。 スパイクタンパク質の迅速な変異がパンデミックの原因の1つと考えられている。
注17)抗原:
ウイルスや細菌など、体内に侵入した際に異物として免疫応答を引き起こす物質を抗原と呼びます。免疫の場合、組換えタンパク質などの抗原を投与することで、抗原に対する抗体を産生します。
注18)IgG+ B細胞:
IgG抗体を細胞表面に発現するB細胞です。
注19)シングルBセル解析:
B細胞を1つずつ単離し、個別に分析することで、B細胞の抗体遺伝子配列を解析します。この遺伝子配列をもとに高い効率で抗体作製が可能となる技術です。
注20)再設計された抗体遺伝子cDNAライブラリー:
TC-mAbマウス由来の免疫組織から取得した軽鎖および重鎖抗体遺伝子cDNAを、定常領域配列と人工的に接続し、軽鎖および重鎖の抗原結合ペアをランダムに組み替えた再設計型抗体遺伝子cDNAライブラリー(シャッフル抗体ライブラリー)を構築しました。これらをCHO細胞内に保持されるマウス人工染色体に搭載することで、安定した再設計抗体ライブラリーとして構築しました。このシャッフル抗体ライブラリーにより、シングルB細胞解析から得られる天然型抗体とは異なる結合特性をもつ人工抗体配列の取得が期待されます。
注21)レパトア解析:
抗体の遺伝子配列はV(D)Jの遺伝子により成り立っています。レパトア解析とは、抗体遺伝子配列の多様性の解析です。
論文タイトル
- 論文タイトル
- A rapid immunization and antibody redesign platform for discovering broadly neutralizing antibodies against non-immunized SARS-CoV-2 variant
(未感作のSARS-CoV-2変異株抗原に対する広域中和抗体が作製できる「迅速な免疫と抗体再設計プラットフォーム」) - DOI
- 10.1016/j.ymthe.2025.10.020.
- 雑誌名
-
Molecular Therapy
論文著者名
Shusei Hamamichi, Narumi Uno, Kazuto Shimoya, Takato Fukushima, Marina Abe, Arata Watanabe, Mizuho Ito, Yuko Wakasa, Yuko Yajima, Rio Suzuki, Natsumi Miyazaki, Akifumi Kamiyama, Kana Uno, Masaharu Hiratsuka, Takashi Moriwaki, Tomokazu Tamura, Kyosuke Kanai, Satoshi Abe, Takasuke Fukuhara, Seiji Kageyama, Masayuki Su’etsugu, Yasuhiro Kazuki*, Kazuma Tomizuka**
*,**:責任著者
研究に関するお問い合わせ
- 香月 康宏(カヅキ ヤスヒロ)
鳥取大学 医学部生命科学科/染色体工学研究センター 教授 -
-
〒683-8503 鳥取県米子市西町86番地
- 0859-38-6219/FAX:0859-38-6210
- kazuki[at]tottori-u.ac.jp
-
- 冨塚 一磨(トミヅカ カズマ)
東京薬科大学 生命科学部 応用生命科学科 生物工学研究室 教授 -
-
〒192-0392 東京都八王子市堀之内1432-1
- 042-676-7139/FAX:042-676-7145
- tomizuka[at]toyaku.ac.jp
-
報道に関するお問い合わせ
- 鳥取大学 米子地区事務部総務課広報係
-
-
〒683-8503 鳥取県米子市西町86番地
- 0859-38-7037/FAX:0859-38-7029
- me-kouhou[at]ml.adm.tottori-u.ac.jp
-
- 東京薬科大学 入試・広報センター
-
- 〒192-0392 東京都八王子市堀之内1432の1番地
- 042-676-4921/Fax:042-676-8961
- 問い合わせフォーム
※メールをご利用の際は、[at]を@に置換してください。









