新型コロナウイルス研究 #03
3CLプロテアーゼ阻害剤の効率的合成および阻害活性評価法の開発
- 薬学部
- 治療薬開発
薬学部 医療衛生薬学科
薬品化学教室 今野 翔 助教
新型コロナウイルスの弁慶の泣き所 -- 3CLプロテアーゼ
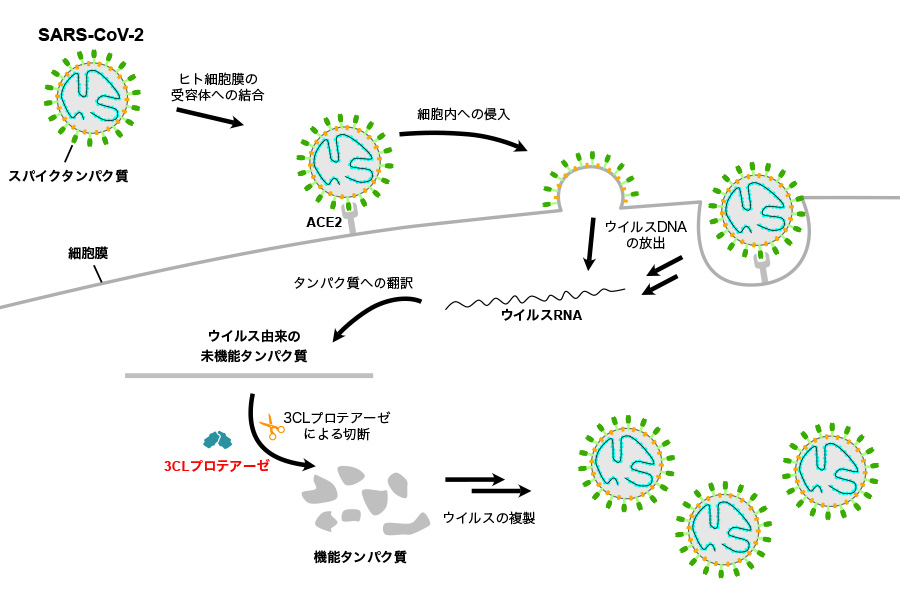
新型コロナウイルス(SARS-CoV-2)はヒトの細胞に侵入したのち、まずヒト細胞内のシステムをハイジャックして増殖を開始します。この増殖過程で、ウイルスは「3CLプロテアーゼ」と呼ばれるウイルス由来のタンパク質分解酵素を利用します。多くのウイルスタンパク質は、細胞の中で作られた段階では機能を持っていません。しかし、3CLプロテアーゼによって切断されると機能をもったタンパク質となり、ウイルスの増殖に関与します。つまり、SARS-CoV-2が増えるために3CLプロテアーゼは必要不可欠な酵素であり、この酵素の機能を止めるとウイルスは増殖できなくなります。また、ヒトは類似の性質を示す酵素をもっていないことから、3CLプロテアーゼは有望な創薬標的といえます。私たちは、2002年のSARS発生時から3CLプロテアーゼ阻害剤の開発を開始しており、2013年に複数の強力な3CLプロテアーゼ阻害剤を報告しています。
 今野 翔 助教
今野 翔 助教
3CLプロテアーゼ阻害剤の大量供給ルートを確立 -- 治療薬開発を少しでも早く
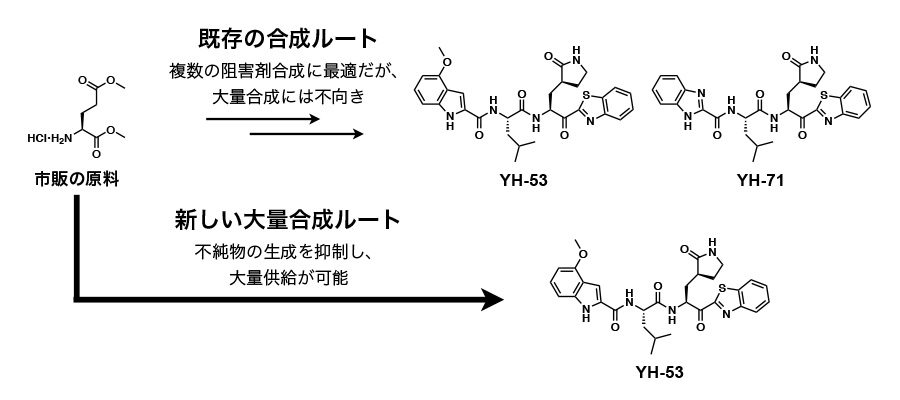
3CLプロテアーゼ阻害剤の合成は、有機合成化学を用いて行われます。阻害剤を作る場合、複数の合成方法の中から目的に合った最適なルートを選択して研究を進めていきます。私たちはこれまで、強力な3CLプロテアーゼ阻害剤の開発を目的にしていたので、様々な種類の阻害剤を効率的に作る合成ルートを採用していました。一方、医薬品開発に向けて安全性や毒性、薬効などの動物試験などを行う場合、一つの阻害剤を大量に用意する必要があります。SARS-CoV-2が突如出現し、治療薬開発が喫緊の課題となり、私たちがこれまでに報告した阻害剤を用いて医薬品開発するには、大量に合成する必要がありました。そこで本事業の支援を受けて動物試験にむけた大量合成ルートの探索を開始しました。これまでの合成ルートでは、目的物と性質の近い不純物を取り除くために高速液体クロマトグラフィーと呼ばれる機械を用いて精製する必要があり、収量の大幅な低下が問題となっていました。新しく開発した合成ルートでは、そのような不純物の生成を劇的に抑制することができ、これまでの方法の数十倍量の3CLプロテアーゼ阻害剤を供給することに成功しました。
化学の力を利用し、阻害活性評価法をより簡便に -- さらに精度の高い阻害剤を
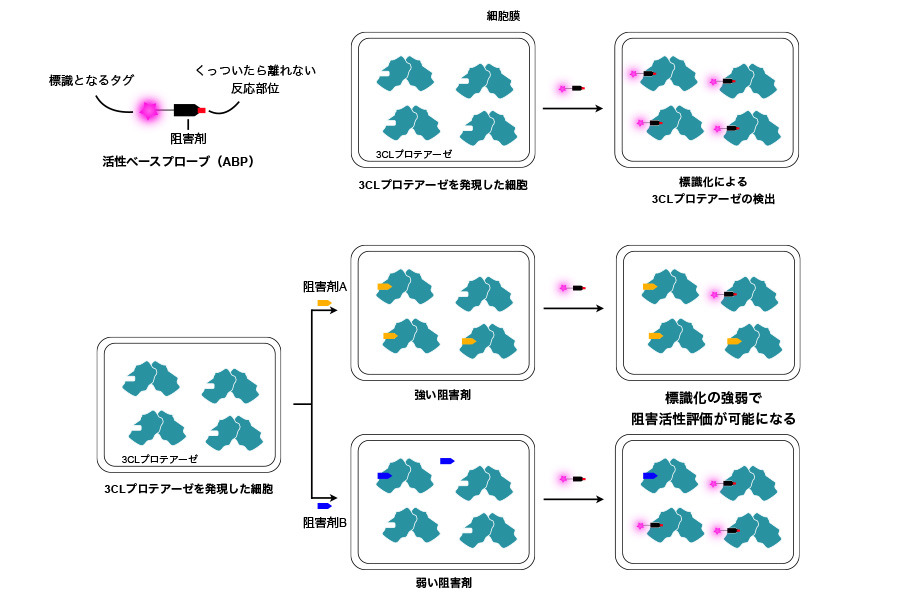
私たちは活性ベースタンパク質プロファイリング(Activity-based protein profiling, ABPP)と呼ばれる方法を用いて、細胞内に存在している3CLプロテアーゼの酵素活性を検出する方法の開発にも挑戦しています。この方法では、私たちがこれまでに開発した阻害剤に「くっついたら離れない反応部位」と「標識となるタグ」を組み込んだ活性ベースプローブ(Activity-based probe, ABP)を設計・合成します。ABPを利用すると、細胞内に存在している活性な状態の3CLプロテアーゼを選択的に標識することが可能になります。
私たちはこの技術を応用することで、細胞内における3CLプロテアーゼ阻害活性評価法の構築をめざしています。すなわち、ABPと3CLプロテアーゼ阻害剤を細胞に処理すると、3CLプロテアーゼはこのどちらかとのみ結合し、ABPによる標識は部分的に阻害されます。ABPによる標識の強弱を様々な阻害剤間で比較することで、細胞膜を透過し、かつ強く3CLプロテアーゼと結合する阻害剤を簡便に探索可能になると期待し、日々研究に取り組んでいます。










