未来医療・共生社会創造人育成プロジェクト『BUTTOBE-NEXT』

概要・背景
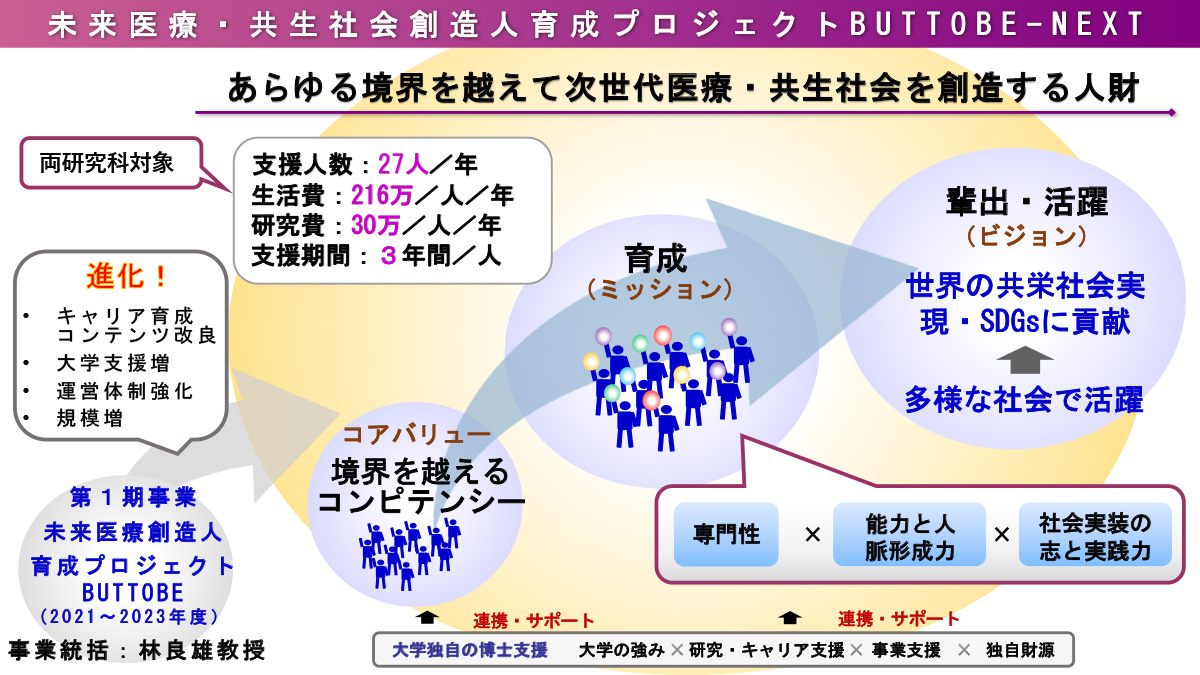
東京薬科大学では、2021年度からJSTのSPRING事業「東京薬科大学 未来医療創造人育成プロジェクト(Beef Up Toyaku Talents to gO BEyond the Borders。以下、BUTTOBE(ぶっとべ)」に取り組んでいます。本プロジェクトは、変革期を迎えた日本の医療を発展させる優秀な博士人財の育成・輩出を目指し、「創薬」、「医療」、「学術」の3コースでキャリア開発・育成コンテンツを学生に提供してきました。これまでの修了生は、大学・アカデミア、企業、病院などで活躍しています。
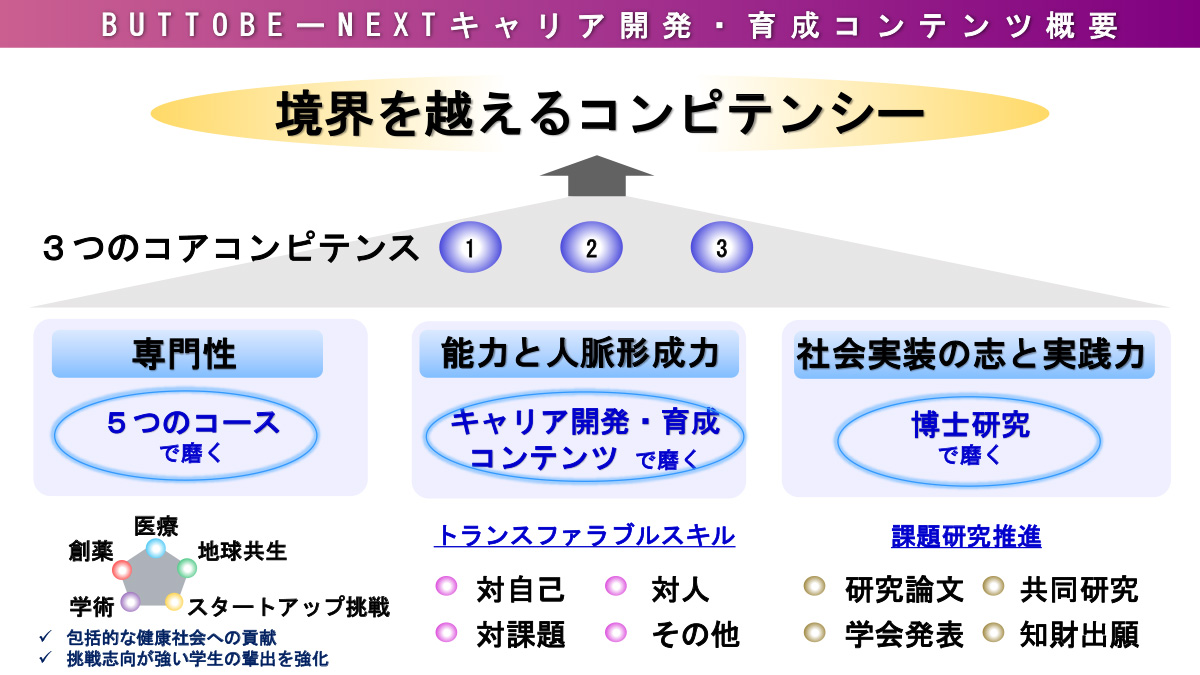
2024年度から新たに「東京薬科大学 未来医療・共生社会創造⼈育成プロジェクト(以下、BUTTOBE-NEXT)(事業統括:降幡知巳教授)」が開始となりました。本プロジェクトでは、新たに「地球共生」、「スタートアップ挑戦」を加えた5つのコースを開設するほか、インターンシップの拡充や大学独自の支援プログラムを追加するなど、従来のキャリア開発・育成コンテンツをさらに発展・拡大させました。本プログラムでは、“境界を超えるコンピテンシーの養成”を目標に、薬学・生命科学の専門を基盤に、共栄社会の実現とSDGsに貢献できる多様な博士人財の輩出を目指します。
お知らせ
- 2026年02月27日
-
BUTTOBE-NEXT Boot Camp2:BUTTOビジネスプランコンペを開催しました
- 2025年12月18日
-
BUTTOBE-NEXT採択学生主催 第3回学内研究発表会を開催しました
- 2025年09月16日
-
BUTTOBE-NEXT 2025 Boot Camp1 Day2を開催しました
- 2025年09月02日
-
BUTTOBE-NEXT 2025 Boot Camp1 Day1を開催しました
- 2025年05月20日
-
BUTTOBE-NEXT 2025 キックオフミーティングが実施されました
- 2024年12月18日
-
第3回 東薬×岐阜薬 次世代研究者挑戦的研究プログラム(SPRING)事業交流会を行いました
- 2024年09月06日
-
BUTTOBE-NEXT 2024 Boot Camp1を開催しました
- 2024年02月09日
-
BUTTOBE 2023 Boot Camp2 ピッチプレゼンを開催しました
未来の医療を担う博士人材たち
未来学術フォアランナー
藤本 陸斗
- 研究科・課程・学年
- 薬学研究科 博士課程1年
- 所属研究室
- 薬品製造学教室
- 研究タイトル
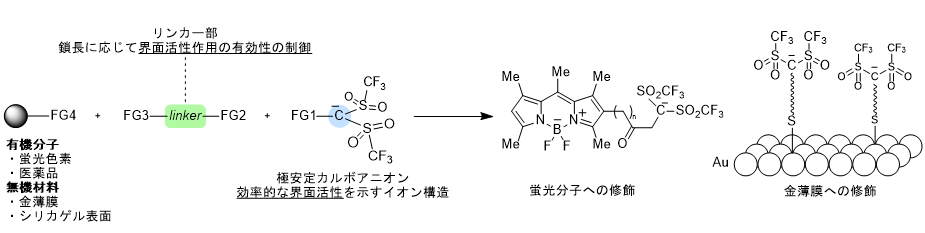
- 極安定カルボアニオンを備えた新規界面活性剤の開発と機能特性の解明
- 研究概要
- 炭素原子上に負電荷をもつカルボアニオンは、一般に不安定で、水中では即座に反応し失活する。一方で、所属研究グループでは、フッ素置換基によって安定化されたカルボアニオンの化学を展開してきた。最近、私は長い炭素鎖を有するカルボアニオン含有塩の優れた界面活性を発見した。本研究では、カルボアニオンと機能性分子を様々な鎖長のリンカーで接続したハイブリッド化合物の開発を試みる。これにより、蛍光分子や医薬品などの有機分子、金薄膜やシリカゲルなどの無機材料に適切な界面活性能を付与し、生体イメージング材料、DDS、表面基材への応用を目指す。

分野横断で挑むイノベーション志向
私は有機化学が可能にする分子レベルのものづくりに魅力を感じ、研究者の道を志しました。将来は異分野にも精通し、グローバルに活躍できる挑戦的な研究者になりたいと考えています。本プロジェクトを通じて独自の発想で新規化合物を創出し、その薬学的特性を見いだすことで、社会に貢献できる機能性分子の開発を目指します。
長田 優也
- 研究科・課程・学年
- 生命科学研究科 博士後期課程2年
- 所属研究室
- 免疫制御学研究室
- 研究タイトル
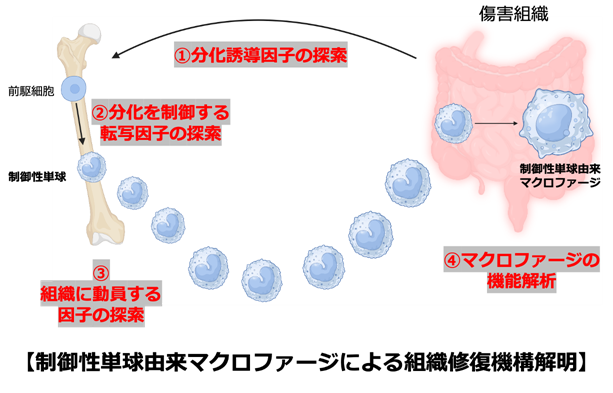
- 制御性単球由来マクロファージの機能解析
- 研究概要
- マクロファージは体内に侵入した病原体を排除するだけでなく、組織の修復や死細胞の除去など、多岐にわたる役割をもつ免疫細胞である。マクロファージの起源のひとつとして骨髄でつくられる単球が知られており、骨髄から出た単球は血液中をめぐり、組織に入ったのちマクロファージへと成熟する。私たちはこれまでに、傷ついた組織を修復する役割をもつ単球を明らかにし、『制御性単球』と命名した。しかし、制御性単球が組織に移行した後、どのように働くかは未解明である。本研究は組織における制御性単球に由来するマクロファージの解析を通して、それらの細胞による組織修復のしくみを解明することを目指す。

既存の概念を粉砕する
私は『デュエリスト』になります。ここでの『デュエリスト』とは、固定観念の打破や既存の知見を覆す発見を通して新たな領域を開拓していく研究者を指します。大学院における研究活動において、私は免疫領域の知見を積み上げてきましたが、未だブレイクスルーとなる発見はできていません。今後は自身の研究領域の枠をこえ、デュエリストとして未知の課題に積極的に挑戦していきます。
関根 舞美
- 研究科・課程・学年
- 生命科学研究科 博士後期課程2年
- 所属研究室
- 生命物理科学研究室
- 研究タイトル
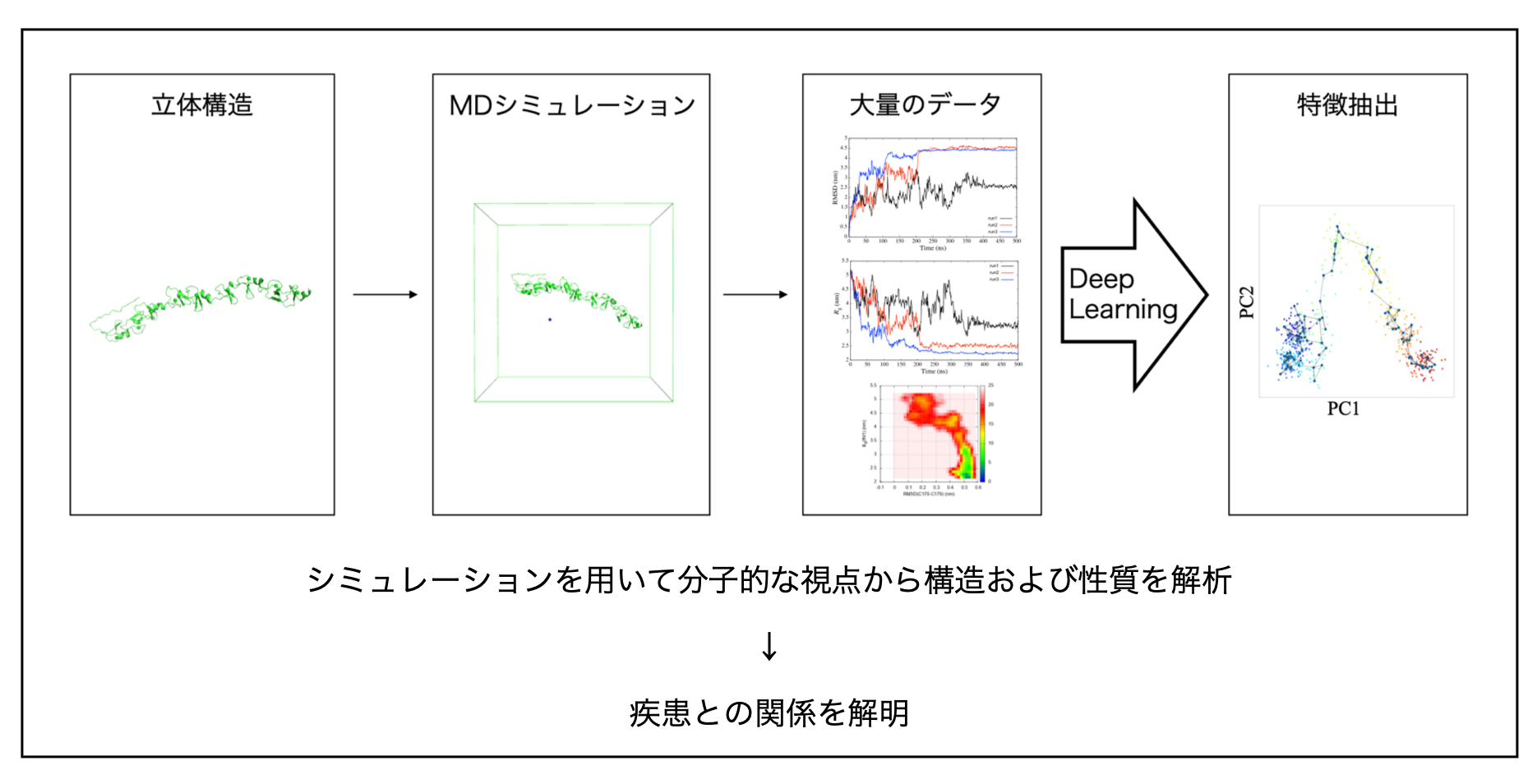
- Deep LearningとMDシミュレーションによる筋疾患関連タンパク質の構造解析
- 研究概要
- FHL1(Four and a half LIM domains 1)遺伝子は、還元小体ミオパチー(RBM)をはじめとするさまざまな筋疾患の原因遺伝子である。FHL1遺伝子にコードされるFHL1タンパク質は、オートファジーやがん抑制などにも関与していることが知られている。ゼブラフィッシュにおいて、fhl1遺伝子の変異と筋疾患の症状の関係についての研究が進められているが、fhl1遺伝子の変異によるfhl1タンパク質の立体構造への影響については報告されていない。そこで、MD(分子動力学)シミュレーションを実行し、野生型と変異型のゼブラフィッシュfhl1タンパク質の立体構造の違いを明らかにする。また、Deep Learningを用いて性質を解析することにより、疾患との関係の解明を目指す。

まだ誰も見たことのないものを見つけにいこう!
コンピュータの性能やAI(人工知能)は日々急速に進歩しており、薬学・生命科学分野においてもこれらを用いたin silicoの研究が取り入れられています。私は、生命科学と情報科学の2つの分野の橋渡しとなる研究者として、学術や医療の発展へ貢献していきます。さらには、誰も見たことのないものを見つけるという研究の楽しさを伝えていくことで科学の普及にも携わっていきたいです。
赤石 佳音
- 研究科・課程・学年
- 生命科学研究科 博士後期課程1年
- 所属研究室
- 幹細胞制御学研究室
- 研究タイトル
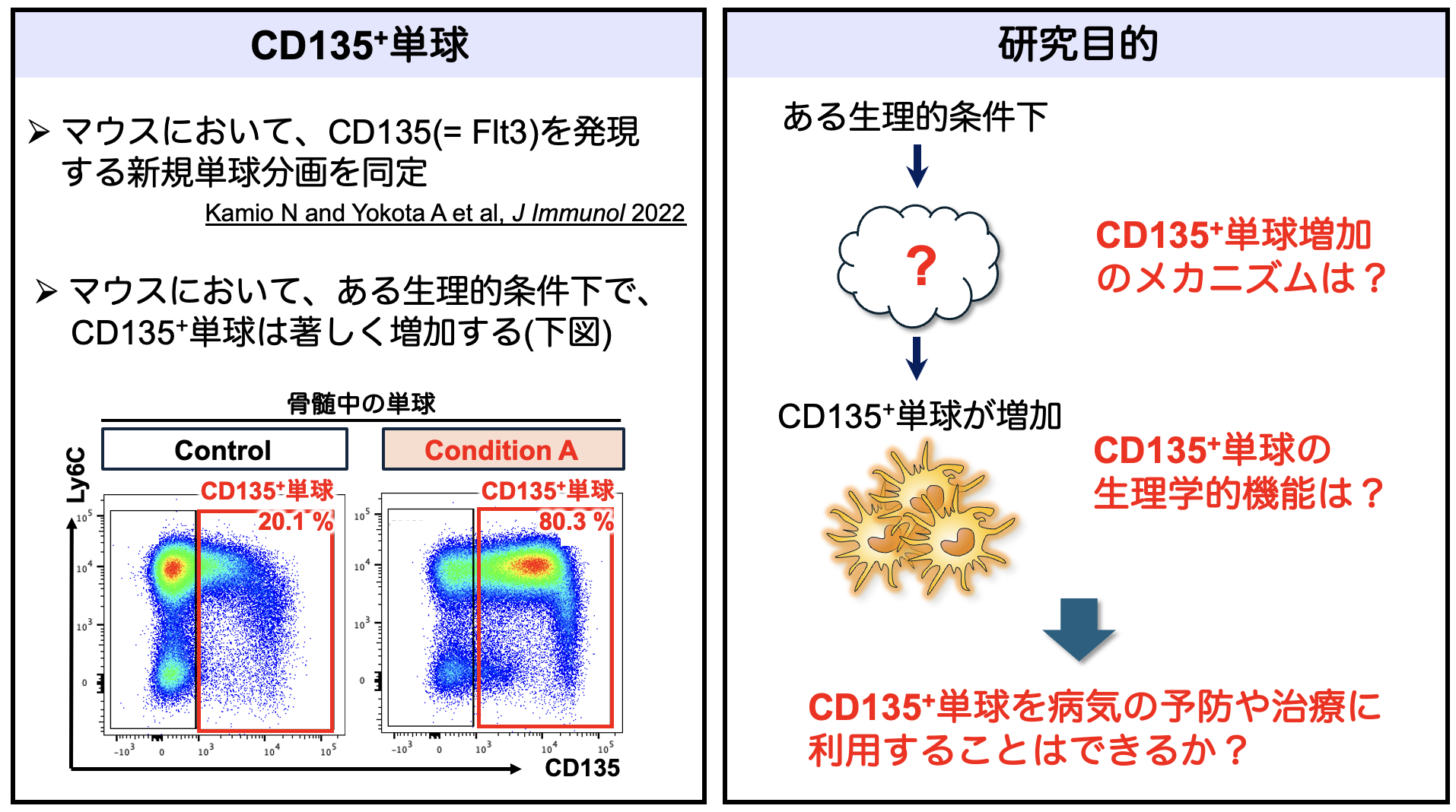
- 新たに同定したCD135+単球分画の分化様式と生理学的機能の解明
- 研究概要
- 単球は、生体防御・炎症制御などを担う白血球分画である。我々は、サイトカインFlt3 Ligandの受容体であるCD135を高発現する新規単球分画を同定した。CD135陽性単球は、従来から知られている単球と樹状細胞両者の機能的特徴を有しているが、それらとは独立した細胞集団である。このCD135陽性単球は、ある生理的条件下において著しく増加することを我々は明らかにしており、この条件下での免疫応答や炎症制御において何らかの重要な役割を担う可能性が示唆される。本研究では、CD135陽性単球の分化制御機構や生理学的機能を解明し、関連する可能性が考えられる様々な疾患の新規治療・予防的アプローチとして、CD135陽性単球を標的とし得る可能性を検証する。

「研究×教育」2本の軸で社会に貢献する
私は、新たに同定された血液細胞が「私たちの体内で何をしているのか」という謎を解き明かすため、日々研究に取り組んでいます。また、学部時代に教職課程を履修し、教育にも強い関心を抱いています。将来的には、新たな発見を積み重ねる「研究者」として、そして子どもたちの探究心を育み、次世代の科学人財を育てる「教育者」として、社会に貢献することを目指します。
田中 美有
- 研究科・課程・学年
- 薬学研究科 博士課程2年
- 所属研究室
- 薬品化学教室
- 研究タイトル
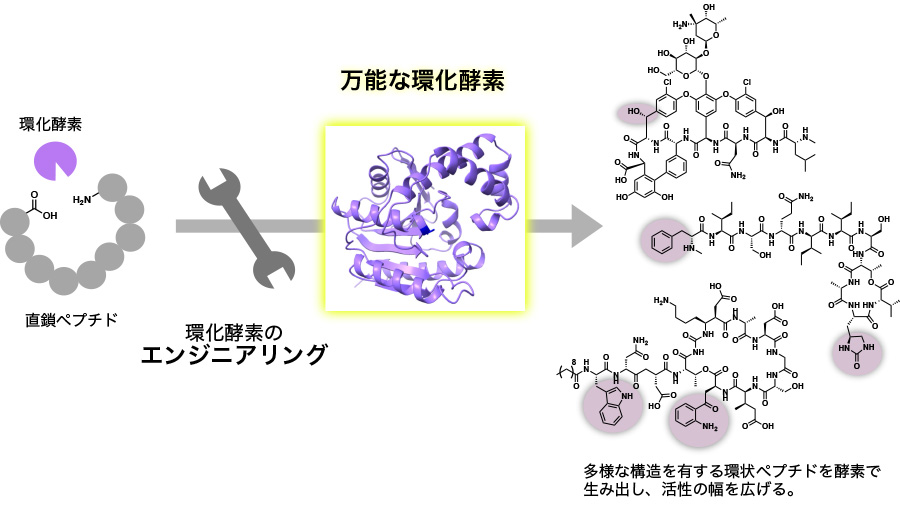
- ペプチド環化酵素の機能解析と誘導体合成への応用
- 研究概要
- 近年、耐性菌出現により抗菌薬の開発に問題が出ています。抗菌薬の中には微生物の二次代謝産物である環状ペプチドが用いられており、それらは微生物内にある生合成酵素の中の「環化酵素」によって環化されます。環化酵素を有効活用することは様々な活性を有する環状ペプチドの創製に繋がります。しかし環化酵素における基質の認識の機序は未だ明らかになっておらず、環化酵素の機能改変に歯止めがかかっています。本研究では、基質と環化酵素の複合体を再現する技術を開発し、環化酵素における基質認識の機序解明を目指します。
カンカコウソは砕けない
私は、生命の生きる知恵を社会へ還元できる仕組みを目指します。生命は生存競争のために驚くべき工夫を施します。もし、我々がその工夫の原理を明らかにできれば、耐性菌やウイルスの出現等、変わりゆく環境の中で、先手を打つことができます。誰かが犠牲になる前に対応し、誰もが健康に過ごせる社会を構築できることを目標に、BUTTOBE-NEXTで邁進して参ります。
北谷 菜津美
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 生体分析化学教室
- 研究タイトル
- 細胞から分泌されるエクソソームのリアルタイム計測技術の開発
- 研究概要
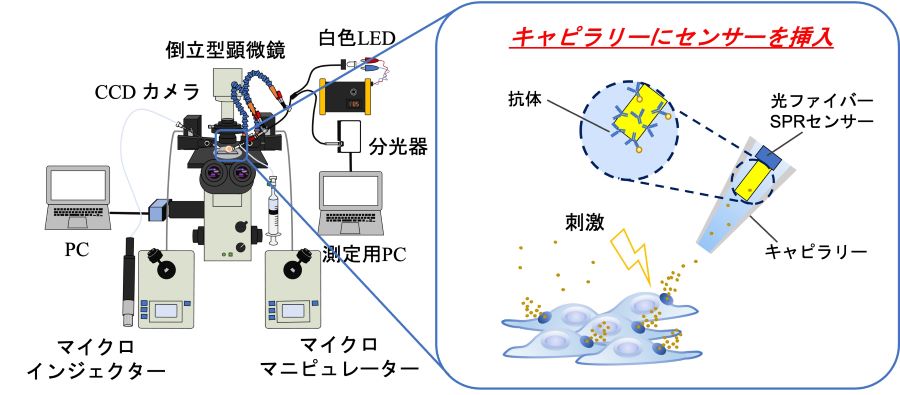
- 刻々と変動する生体高分子の動態を定量的に計測することは生命現象を理解するために必要とされる。本研究では、細胞から分泌されるエクソソームを拡散希釈される前に細胞近傍で計測できるシステムを開発する。本計測技術では、エクソソームの動態をリアルタイムで計測できるため、細胞を化学物質や脱分極の刺激を付与した際に、細胞がどのくらいの時間で、どのくらいの個数のエクソソームを分泌したのか明らかにできる。技術開発に求められる要素は、細胞近傍に接近させることのできる微小センサーの開発とリアルタイム計測が可能な技術であり、これを達成するために光ファイバー表面プラズモン共鳴(SPR)センサーに着目した。

計測で切り拓く科学の未来
計測技術の限界に突き当たると、科学および産業の進展は止まってしまいます。しかしながら、計測技術が十分に発展してきた現在においても、計測技術に限界があります。このような社会背景に鑑みて、計測できないものを計測できるような研究者を目指します。分析技術の開発を通して、学術や産業の発展、ひいては社会に貢献します。
兒嶋 洸貴
- 研究科・課程・学年
- 生命科学研究科 博士後期課程3年
- 所属研究室
- 再生医科学研究室
- 研究タイトル
- 異種間キメラにおける自己免疫反応および免疫寛容機構の解明
- 研究概要
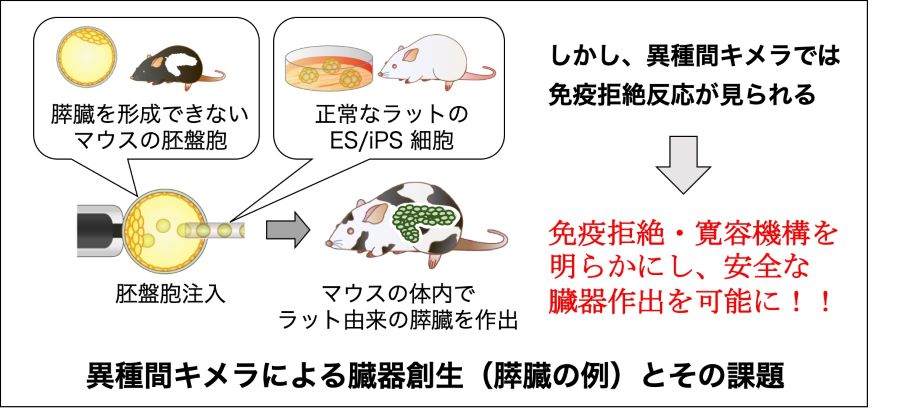
- 動物の発生環境を利用した臓器作製法は、現在のところ多能性幹細胞から完全に機能的な臓器を作出できる唯一の方法である。しかし、異種の臓器をもつキメラ動物では1型糖尿病様の血糖値上昇や重度の皮膚炎など、自己免疫疾患様の症状が確認されている。キメラ動物で見られる免疫反応に関して、これまで詳細な解析はされておらず、動物体内での安全な臓器作製法の確立における一つの壁となっている。本研究では、様々な系統のラット-マウス異種間キメラを用い、新たな免疫寛容誘導システムの詳細を明らかにする。本研究は免疫学の新たな知見の獲得のみならず、臓器創生・移植治療の分野に大いに貢献できると考えられる。

研究を新たな医療に昇華する
iPS細胞の発見から再生医療は目覚ましい発展がなされており、iPS細胞由来のミニ臓器や心筋シート、網膜色素細胞のin vitroでの作製が報告されています。私はそれに続くブレイクスルーとして、機能的なヒト臓器の創生を目指して取り組んでいきます。そして将来的には研究と本プロジェクトで得られた知見を活かし、基礎研究を新しい医療に繋ぐ研究者として先進医療に貢献していきたいです。
佐藤 圭恭
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 薬物動態制御学教室
- 研究タイトル
- トランスポーターを介した臓器連関の解明
- 研究概要
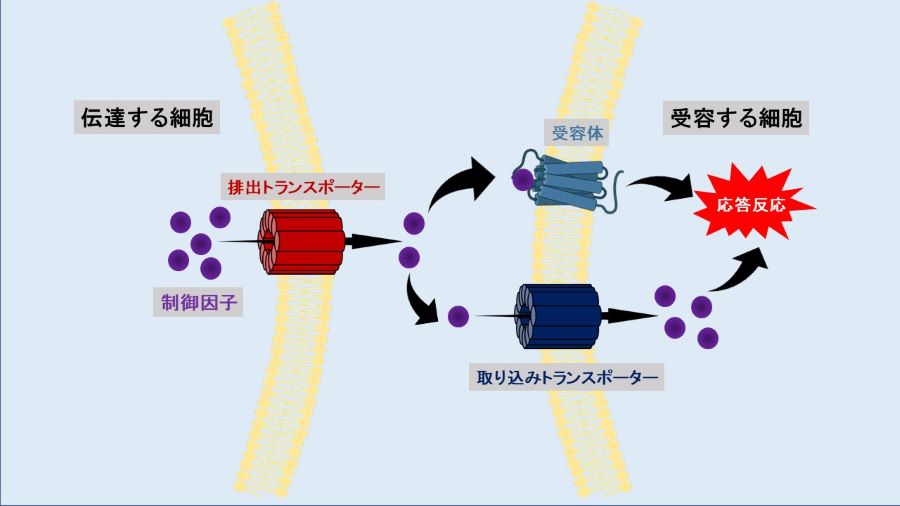
- 臓器連関とは、細胞と細胞、あるいは組織や臓器との間で行われる恒常性を維持するための情報交換機構です。古くから、臓器間の情報伝達は、ホルモンや神経伝達物質などの制御因子とそれらに対する受容体を介して行われることが知られていましたが、最近では、制御因子を標的細胞内へ送達することで情報伝達を行う機構の存在が明らかになりつつあります。本研究では、臓器連関における制御因子の膜透過を制御するトランスポーターを同定することで、制御因子の膜透過を説明し、臓器連関の詳細なメカニズムの解明に取り組みます。

新たな常識を創造する
私は将来、アカデミア研究を通じて学問にパラダイムシフトを起こすような研究者になりたいと考えています。薬学や生命科学は、今までに積み上げられてきた数々の知見に基づく一方、その常識とされるものの中には根拠が不明確なものもあります。そのような常識にとらわれることのない、柔軟な着想を基に新たな常識を創造することで、医療の発展に寄与できるような研究をしていきたいです。
未来創薬イノベーター
吉原 昂洋
- 研究科・課程・学年
- 薬学研究科 博士課程2年
- 所属研究室
- 臨床微生物学教室
- 研究タイトル
- 「薬剤耐性菌を感受性菌に戻す」感染症治療を革新する薬剤の開発
- 研究概要
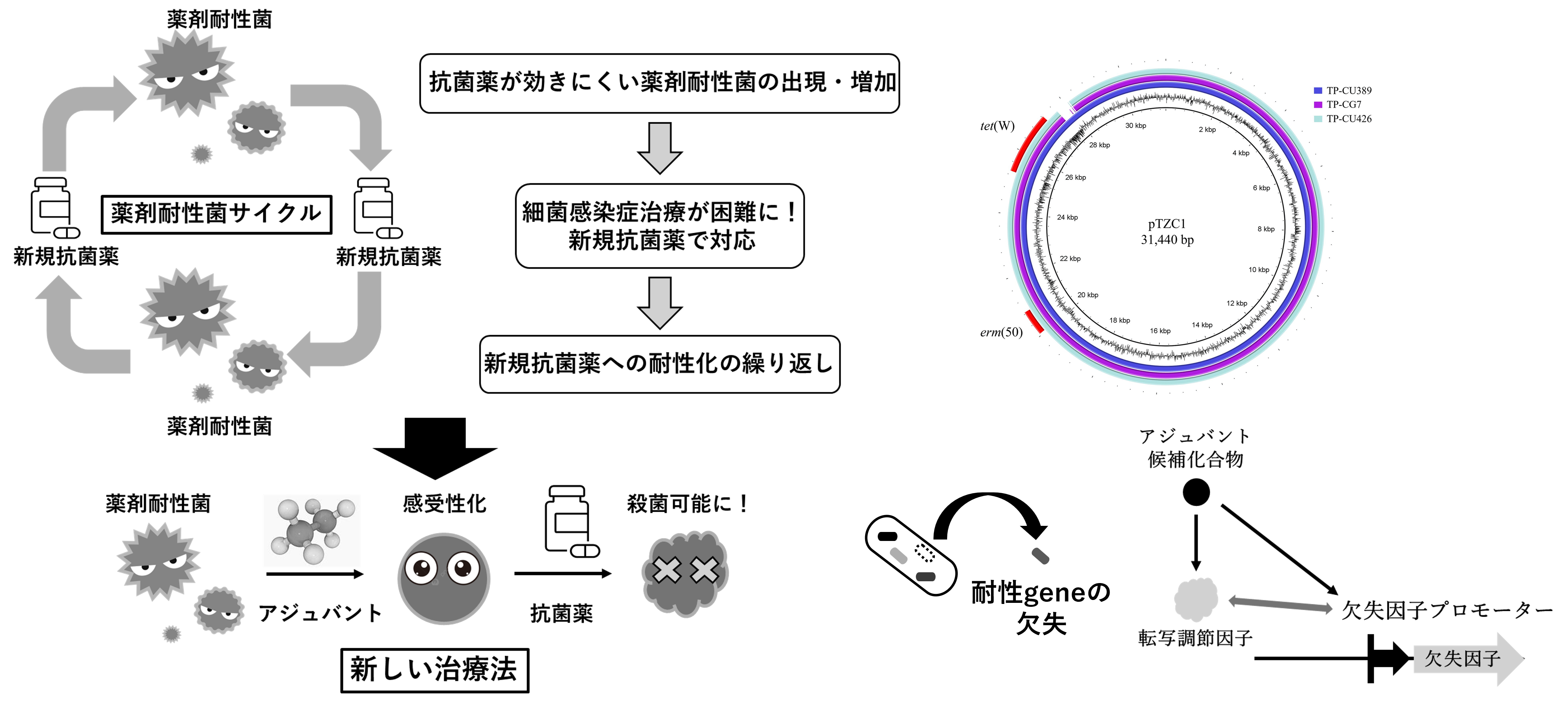
- Cutibacterium acnes (アクネ菌) は、ざ瘡 (ニキビ) だけでなく、サルコイドーシスや前立腺がんなどの慢性疾患の起炎菌とされている。近年、抗菌薬に耐性を獲得した薬剤耐性菌が増加しており、治療の難渋化など臨床上問題となっている。本研究では、薬剤耐性アクネ菌によるニキビに対して、これまでにない全く新しい治療法を開発する。これを実現するため、臨床分離株を用いて、耐性遺伝子の欠失因子を同定、誘導する化合物を探索する。本研究成果は、他の薬剤耐性菌感染症治療にも応用できると考えられ、これまでの感染症治療を革新する。

薬が効く世界を、もう一度
近年、抗菌薬の効かない薬剤耐性菌が世界中で蔓延している。耐性菌に対して、様々な対策がなされている中、私は逆転の発想で「効かなくなった薬を、再び効かせる」ことを目指し、耐性菌の感受性化に取り組んでいます。見過ごされがちな菌の変化を捉え、感染症治療の可能性を広げる研究を進めています。本研究および本プロジェクトを通じて、感染症で苦しむ人々を救う研究者を目指します。
佐志 陽菜実
- 研究科・課程・学年
- 薬学研究科 博士課程1年
- 所属研究室
- 応用生化学教室
- 研究タイトル
- 抗LRP1抗体による正常眼圧緑内障治療システムの構築
- 研究概要
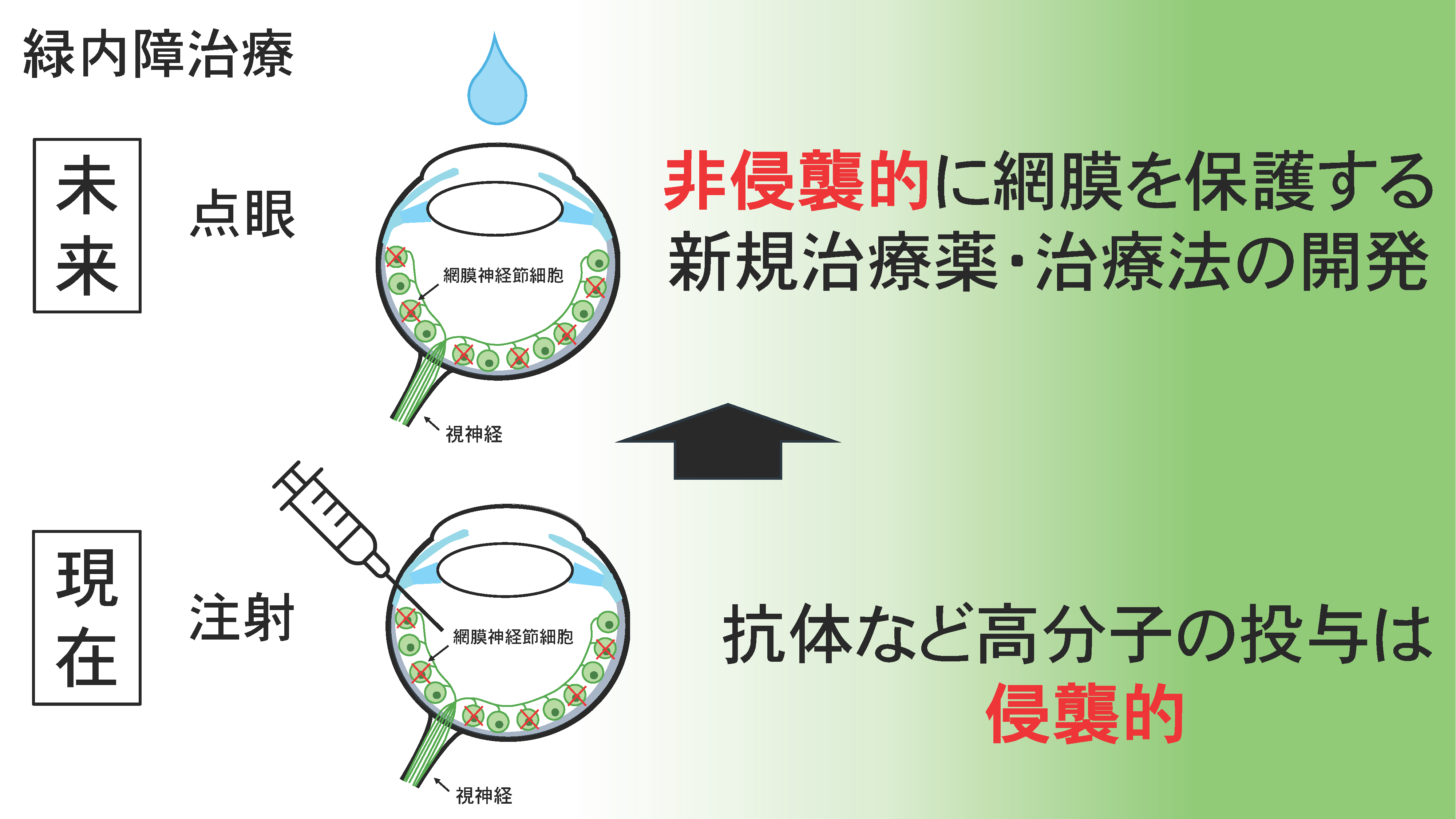
- 緑内障は日本の失明原因疾患第1位であり、その約7割を占める正常眼圧緑内障は治療薬の効果が乏しく、新規治療薬が渇望されている。これまでに我々は、網膜神経節細胞の低密度リポタンパク質受容体関連タンパク質1 (LRP1) を介した神経保護機構を明らかにし、この効果を発揮する抗体の作製に成功した。しかし、現時点で抗体による眼疾患治療は侵襲的な硝子体内注射に頼らざるを得ない。本研究は注射を必要としない抗LRP1抗体を用いた正常眼圧緑内障治療システムの構築を目的とする。ここで得られた成果は、新規緑内障治療の実現と同時に、眼疾患治療の変革と発展に寄与すると信じる。

誰かの“見える”を守るために、視神経と本気で向き合う!
『今視ている光景が少しずつ失われていったら…。』 もし、そんなことが起こったらどう感じますか? 私は、加齢とともに発症リスクが高まる緑内障 (正常眼圧緑内障) の新規治療システムの構築を進めています。近年目覚ましい開発が進む抗体などの高分子による眼疾患治療は、侵襲的な硝子体内注射に頼らざるを得ません。そこで、注射を使用せずに網膜を保護する治療薬・治療法を開発し、社会に貢献します。
大平 京典
- 研究科・課程・学年
- 薬学研究科 博士課程1年
- 所属研究室
- 薬品化学教室
- 研究タイトル
- 難治性筋ジストロフィー新規治療戦略を目指したCDP-リビトール誘導体の創製
- 研究概要
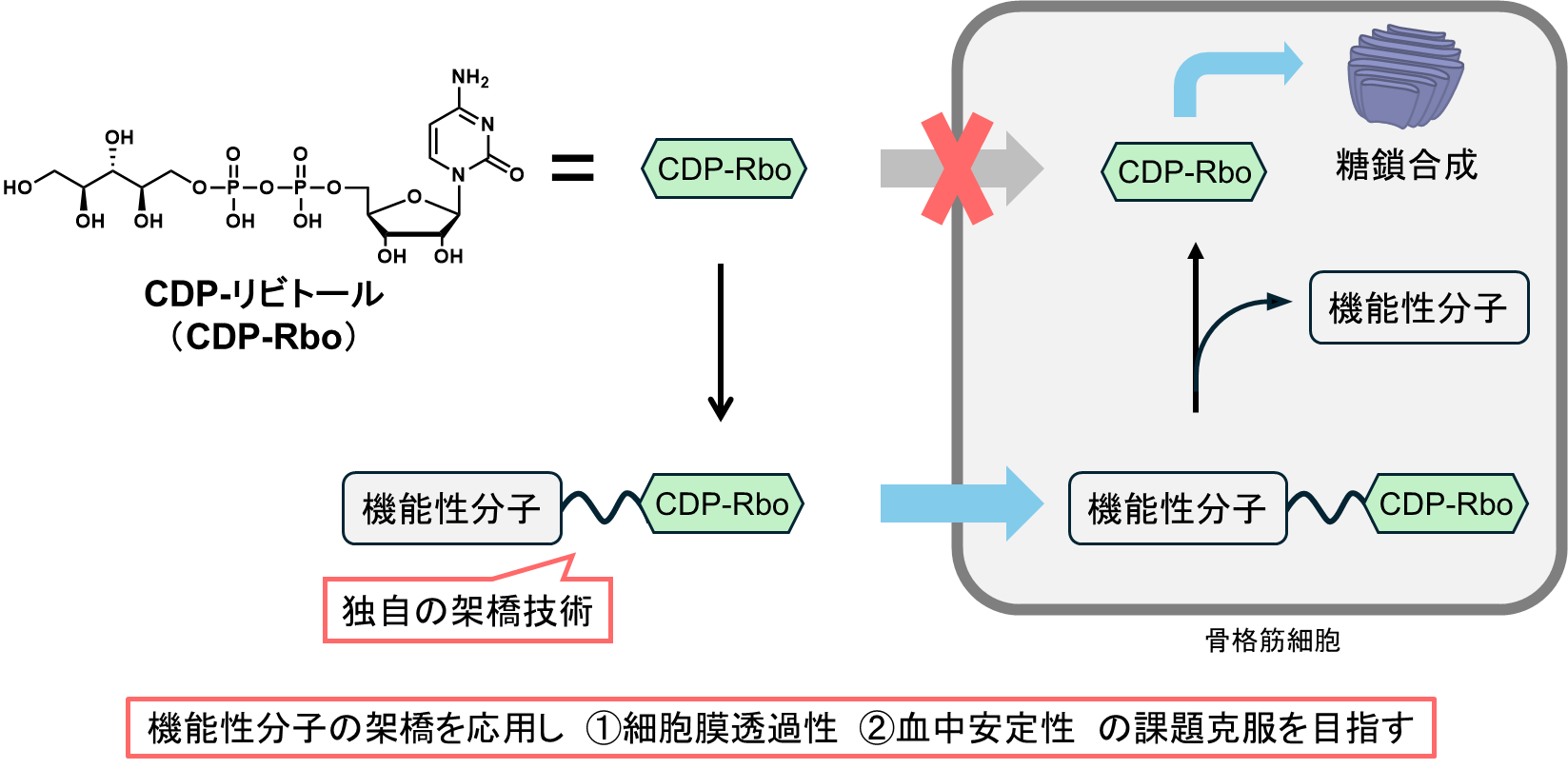
- 骨格筋細胞におけるα-ジストログリカンの糖鎖修飾異常は、難治性の糖鎖異常型筋ジストロフィーを引き起こす。この異常は主要な糖鎖修飾酵素の変異により生じる。近年、これら酵素の基質であるCDP-リビトールを細胞内に補充することで正常糖鎖を回復させる可能性が示唆された。この「基質補充療法」を実現させるため、CDP-リビトールの低い細胞膜透過性と血中安定性を克服する必要がある。本研究では課題克服のため、機能性分子を架橋したCDP-リビトール誘導体を創製することで、難治性疾患に対する新規治療戦略の実現を目指す。

知識・技術・想いを紡ぎ、置き去りの難病に挑む
医療技術が飛躍的に進歩する現代でも、治療法がない疾患は依然として多く存在します。そんな先進医療から「置き去り」にされた人々を救うため、私は化学の力を用いた革新的治療法開発に挑みます。そして、本プロジェクトを通じて多くの知識や技術、そして想いを集約させ、大きな力で難治性疾患の壁を打ち破り、一人でも多くの人に明るい未来を届けることを目標に日々精進してまいります。
根岸 由佳
- 研究科・課程・学年
- 薬学研究科 博士課程2年
- 所属研究室
- 創薬基盤科学教室
- 研究タイトル
- 活性化アストロサイトを伴う神経障害を再現したパーキンソン病型ヒト脳モデルの開発
- 研究概要
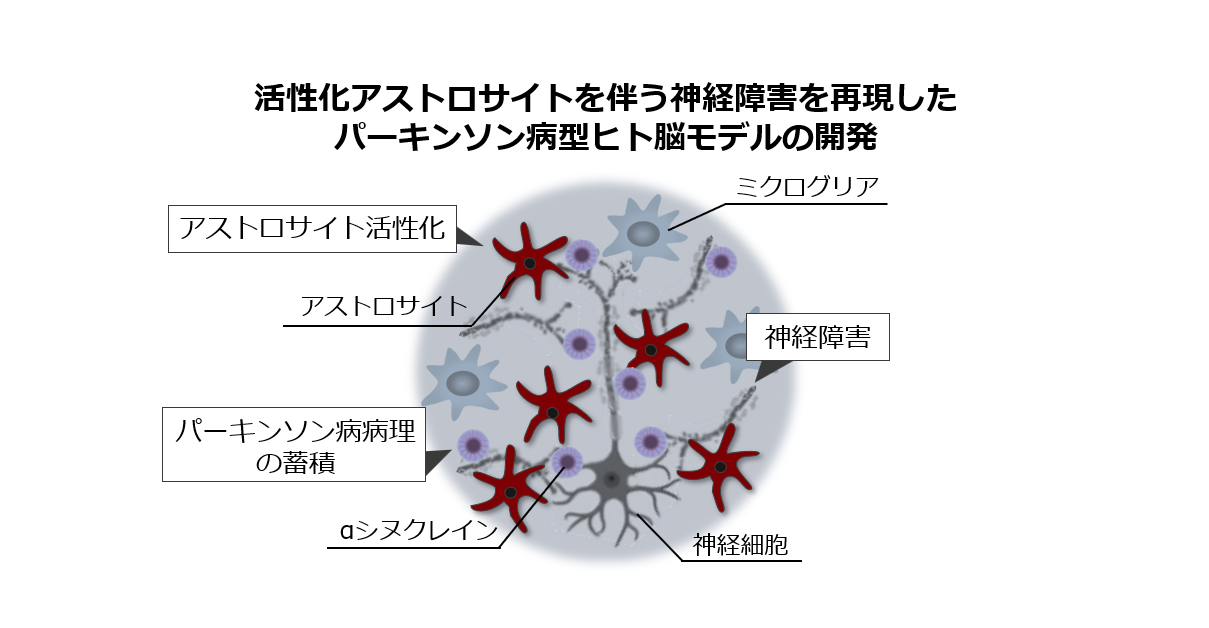
- パーキンソン病(PD)は未だ有効な治療法がない。近年、新たな治療標的として活性化アストロサイトが注目されている。しかし、その関与を創薬研究において評価するための適切なin vitroモデルは確立されていない。本研究では、ヒト不死化脳細胞と3次元スフェロイド培養技術を組み合わせ、アストロサイトの活性化を伴う神経障害を再現する新たなPDモデルの開発を目指す。本手法は、生体内の複雑な細胞間相互作用を模倣し、高い病態再現性と創薬への応用性を両立させる。本モデルは、PDにおける活性化アストロサイトの役割解明を促進し、グリア細胞を標的とした革新的な治療法開発を加速させることが期待される。

脳疾患の謎を解き、治療の未来を照らす
近年、医療の発展速度は著しいですが、ヒトの複雑な病態という『謎』のために、中枢神経系疾患治療薬開発は難航しています。私は、アストロサイトの活性化に着目し、神経とアストロサイトの複雑な相互作用を含めて再現する、新たなヒト脳疾患モデルの開発に挑戦します。この研究基盤で病態の謎を解き明かし、創薬研究そのものを加速させることで、多くの患者に希望を届ける未来に貢献します。
海老澤 歩果
- 研究科・課程・学年
- 薬学研究科 博士課程1年
- 所属研究室
- 創薬基盤科学教室
- 研究タイトル
- 創薬研究に有用な階層×コアシェル型in vitroグリオーマモデルの開発
- 研究概要
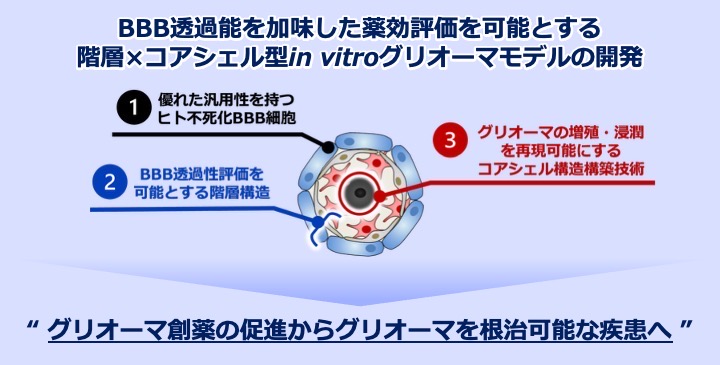
- グリオーマは脳に発生する悪性腫瘍であり、高い悪性度で5年生存率が10%以下であることから、早急な新規治療法の開発が求められている疾患である。グリオーマに対する新規治療法は多岐にわたって検討されているが、臨床での応用に至った治療薬は未だない。この創薬研究促進のため、本研究ではグリオーマの病態再現と治療効果解析に有用な階層×コアシェル型in vitroヒトグリオーマモデルの構築に取り組む。本モデルの開発により、病態メカニズム解明から薬効評価までを一貫して行うことを可能とし、新規グリオーマ治療薬開発期間の大幅な短縮、ひいては治療法開発の新たな基盤を築くことが期待される。

まだないなら、創るしかない
私は創薬研究を通して“治せない病気”を減らし、助かる命を増やすことをミッションとし、グリオーマの新規治療薬開発に向けた評価系の開発に取り組みます。本研究によって、今までになかったグリオーマを根治することのできる未来を『創る』ことを目標に、本研究の遂行とBUTTOBE-NEXTプログラムを最大限活用し、研究者としてのさらなる成長を目指します。
池川 馨
- 研究科・課程・学年
- 薬学研究科 博士課程2年
- 所属研究室
- 薬品化学教室
- 研究タイトル
- ON / OFFスイッチ型光反応性基を用いた生体適応型タンパク質修飾法の開発
- 研究概要
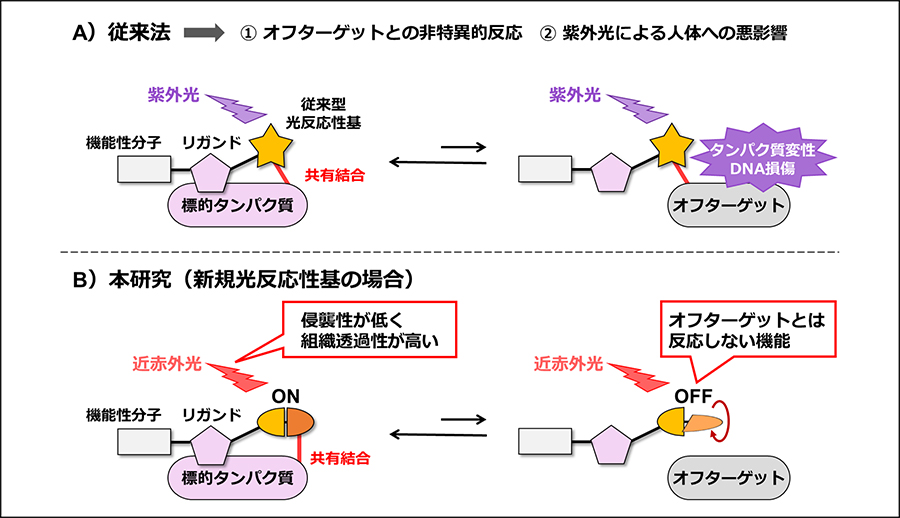
- タンパク質化学修飾法の中でも、光によりタンパク質と共有結合を形成する光反応性基を用いた手法は、生命科学・創薬研究で汎用される手法である。しかし、非特異的反応や高侵襲性の紫外光によるタンパク質変性、DNA損傷などの問題があり、生体内応用には至っていない。本研究では、標的と結合時のみ光架橋反応を起こすしたON / OFFスイッチ機能、そして低侵襲性かつ組織透過性の高い近赤外光による励起特性を兼ね備えた新規光反応性基を開発する。さらに、新規光反応性基による標的タンパク質修飾の有用性を示すと共に、光を用いた新たな創薬モダリティーの確立を目指す。
『つなぐ』で叶える明るい未来
私は、光化学とペプチド化学を専門に創薬研究を行ってきました。本研究では、これまでに培った技術を活かし、『つなぐ』をテーマに新規創薬モダリティーの開発に挑戦します。本研究が「分子」だけでなく、異なる「分野」や多くの「人」をつなぎ合わせ、明るい未来が実現することを目標に尽力します。そして、本研究とBUTTOBE-NEXTプログラムを通して、研究者としても大きく飛躍してみせます。
櫻井 諒一
- 研究科・課程・学年
- 生命科学研究科 博士後期課程2年
- 所属研究室
- 生物工学研究室
- 研究タイトル
- ゲノム編集誘導性分子多様化によるタンパク質分解誘導抗体の表現型スクリーニング
- 研究概要
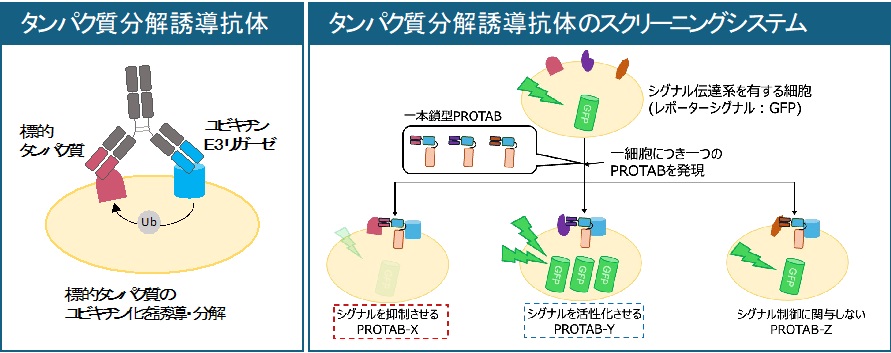
- 細胞膜受容体を標的とする薬剤は様々な疾病の治療薬となり得るが、構造が複雑な受容体を1つの結合分子で制御することは難しい。近年、ユビキチンE3リガーゼと標的受容体に結合し、後者を分解するタンパク質分解誘導抗体(PROTAB)が注目されているが、表現型スクリーニングが困難という点がPROTABを含めた抗体創薬の課題である。本研究では、哺乳動物由来の培養細胞上で抗体選抜が可能なMammalian Displayシステムを発展させ、増殖シグナルレポーター遺伝子をもつ多様化PROTABディスプレイライブラリを構築し、標的の特定を必要としないがん治療候補抗体の取得を目指す。
道無き道を行く
私を研究者としての道に誘った抗体は低分子に次ぐモダリティですが、近年では標的分子の枯渇や開発の鈍化などの課題に直面しています。私は従来アプローチでは取得困難である機能抗体の表現型スクリーニングシステムの構築に取り組み、抗体創薬に取り巻く現状の打破を試みます。将来的には抗体だけでなく、様々な創薬プロセスを根本から変えるような革新的な技術創出に貢献できる研究者を目指します。
松村 清香
- 研究科・課程・学年
- 薬学研究科 博士課程2年
- 所属研究室
- 応用生化学教室
- 研究タイトル
- 血管性認知症の病態形成における脳血管周囲マクロファージの役割の解明
- 研究概要
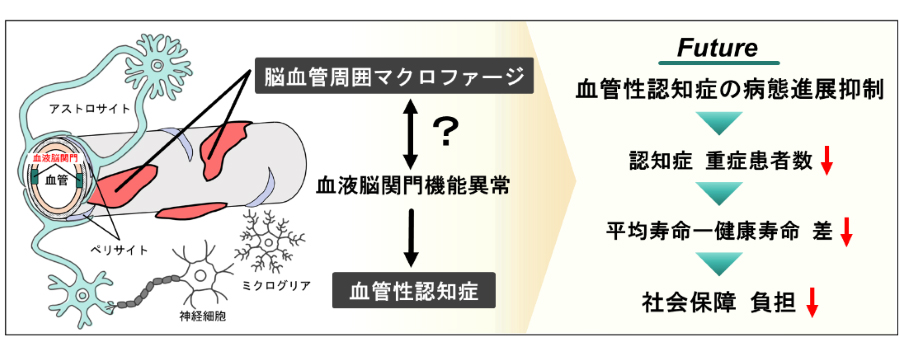
- 血管性認知症の病態形成には、脳への物質侵入を厳密に制御する血液脳関門を含む神経血管周囲環境の機能破綻が関与する。組織恒常性に関わる組織常在マクロファージの1つである脳血管周囲マクロファージは、神経血管周囲環境の機能維持に関わると考えられるが、その役割の詳細は不明である。そこで本研究では、血管性認知症モデルマウスを用いて、脳血管周囲マクロファージの詳細な生理学的機能および脳血流量低下を原因とする血管性認知症の病態進展との関連性を明らかにすることを目的とする。また、脳血管周囲マクロファージを含めた神経血管周囲環境のin vitroモデル開発とその応用により、新たな治療薬開発を目指す。

“難治”を“根治”へ
医療の進歩が目覚ましい今日においても、適切な治療が存在せず、病態の悪化・長期化に苦しむ患者が多く存在します。このような状態を打開する一手を自身で見出すために、私は難治性疾患研究の道を志しました。今日の医療は、試行錯誤を繰り返しつつ、一歩一歩成果を積み上げてきた先駆者の努力の結晶です。これらと先端的な発想を組み合わせることで “難治”性疾患が“根治”疾患となる未来を目指します。
山内 勇輝
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 薬品化学教室
- 研究タイトル
- 薬剤耐性菌に対する新規治療戦略を指向したタンパク質分解誘導薬の開発とその応用
- 研究概要
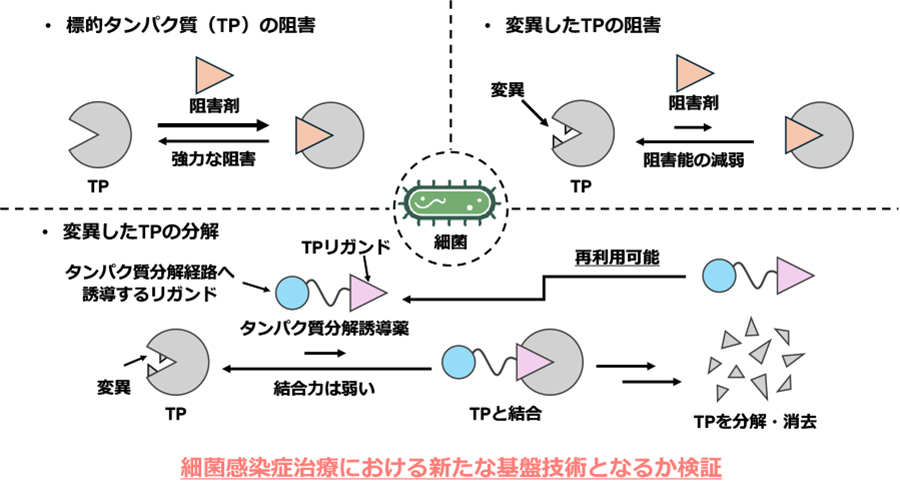
- 薬剤耐性菌の急速な増加は、既存抗菌薬の効果低下や新規抗菌薬開発・承認の劇的な遅れが原因の一つである。この課題の根本的解決には新たなメカニズムで作用する抗菌薬が必要である。最近、タンパク質分解誘導薬を利用した標的タンパク質分解(TPD)が注目されており、標的タンパク質が変異した場合にもTPDを可能とする。従って、細菌に対するタンパク質分解誘導薬の創製が、薬剤耐性菌に対抗するブレイクスルーになる可能性がある。本研究では、アシルデプシペプチド系抗生物質を利用した細菌のタンパク質分解誘導薬を創製し、細菌感染症に対する新たな治療戦略への展開を目指す。
分子に込めた情熱が、新たな治療を生む
私は、化学の力を活用して、創薬の視点から社会に貢献したいと考えています。化学の最大の魅力は、自ら創出した分子が新薬として期待される点にあると思います。新薬の創出は非常に険しい道です。しかし、可能性がゼロでない限り努力し、挑戦し続けることが私の使命だと考えています。最終的には、アンメットメディカルニーズの解消に繋がる分子を創り出し、自らの研究を通じて社会貢献に挑戦します。
大木 聖矢
- 研究科・課程・学年
- 薬学研究科 博士課程4年
- 所属研究室
- 創薬基盤科学教室
- 研究タイトル
- 希少疾患創薬の活性化を指向した新規ヒト脳モデルの開発
- 研究概要
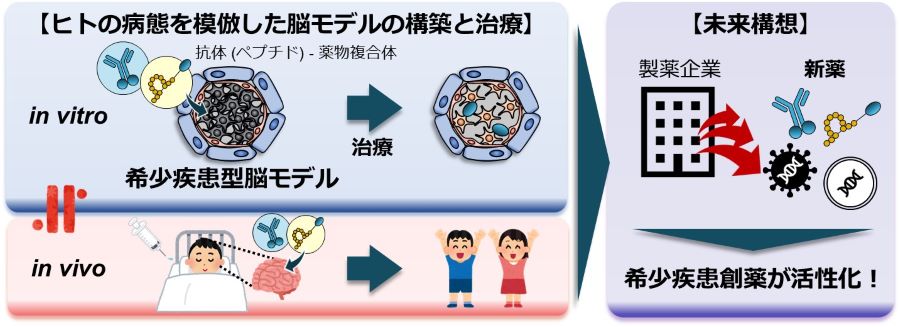
- 先天性希少疾患は、患者数が少なくマーケットが小さことから、製薬企業が創薬に最も取り組みにくい疾患の1つです。特に、中枢症状に対しては、血液脳関門を透過して脳内へ移行できる医薬品がなく、ここに大きなアンメットメディカルニーズがあります。本研究では、希少疾患型ヒト脳モデルを開発し、さらにその治療用高分子の脳移行性と薬効の同時評価への応用までを実証することを目的とします。本モデルを用いることで、ヒト外挿性のある薬物の脳移行性と薬理効果の同時評価をできることが明らかとなります。本研究成果は、希少疾患創薬の活性化に繋がることが期待されます。

脳研究, NO LIFE
私は、成果をもって、社会を変え続ける研究者を目指します。ここでの社会とは先天性希少疾患の創薬研究に取り組みやすい社会を指します。このような社会を実現させるために、本研究テーマを足掛かりに、希少疾患創薬のあり方を変える、そんな研究を進めてまいります。また、将来は研究領域全体の戦略を立て続けることを仕事としたいと考えています。今は、研究者としてまだまだ未熟ですが、研究テーマやBUTTOBE-NEXTの多彩なプログラムを通して、BUTTOBE-NEXT採択期間に大きく成長してみせます。
松沼 真澄
- 研究科・課程・学年
- 薬学研究科 博士課程4年
- 所属研究室
- 病態生化学教室
- 研究タイトル
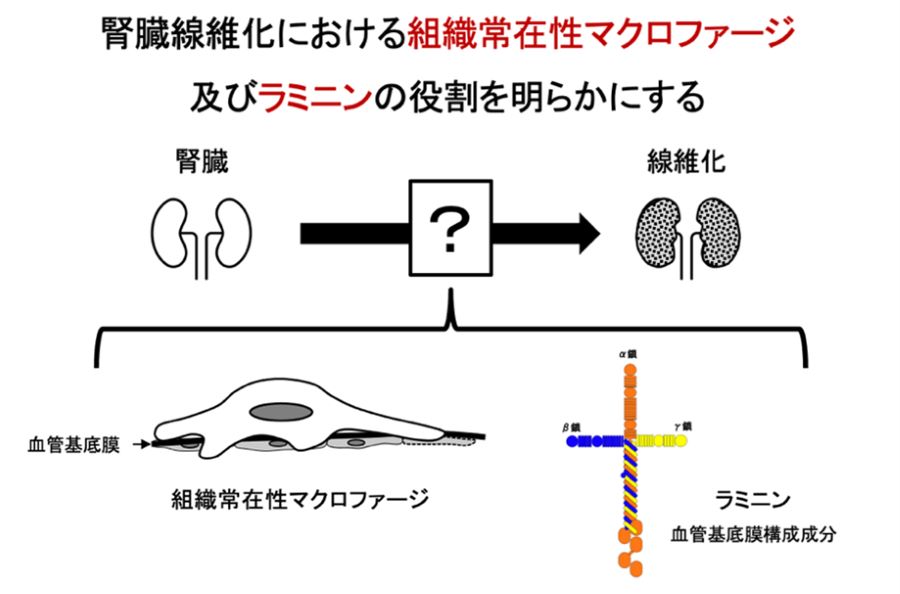
- 腎臓の線維化における組織常在性マクロファージおよびラミニンの役割の解明
- 研究概要
- 腎臓の線維化は、慢性腎臓病に見られる共通の組織所見である。腎臓だけでなく、線維化した組織の機能回復は高いアンメット・メディカル・ニーズであり、抗線維化に向けたメカニズムの解明が求められている。これまでに、組織常在性マクロファージが線維化に至るプロセスの鍵となることが明らかになっているが、そのメカニズムは十分に解明されていない。最近、組織常在性マクロファージが尿細管周囲の血管基底膜に接着しており、活性化に伴って血管障害をもたらす可能性が示された。本研究では、腎臓の線維化において鍵となる組織常在性マクロファージと尿細管周囲の血管基底膜に含まれるラミニンの役割を明らかにする。

一つひとつ堅実に前進
私が研究に取り組む原点は、治療困難な疾患の発症機序の解明および治療薬の探索を通じて患者のQOLを向上させるより良い医療を提供することにあります。組織線維化は、様々な器官の機能不全に関与するため、関係する患者数の多い病態の一つです。しかしながら、現在、線維化した組織を修復する有効な治療薬は存在しません。私は最先端の技術や手法を習得し、新しい知見を生み出すことで、組織線維化を克服することを目標としています。研究成果を通し組織線維化のもたらす疾患や社会的負担を広く伝えることで、医療現場や医療制度に貢献することを目指します。
村野 周子 アンバー
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 薬品化学教室
- 研究タイトル
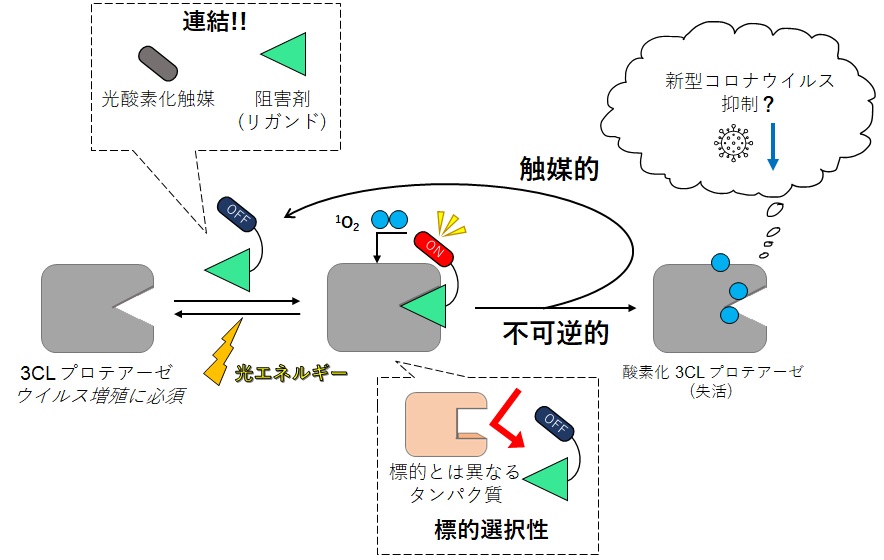
- SARS-CoV-2 の 3CL プロテアーゼを選択的に光酸素化する触媒-リガンドコンジュゲートの開発
- 研究概要
- 新型コロナウイルス (SARS-CoV-2) の 3CLプロテアーゼ (3CLpro) はウイルスが細胞内で複製されるのに必須であり、その不活化剤は SARS-CoV-2 の治療薬となる。この3CLpro を不活化する新しい方法として、我々は光酸素化に着目している。光酸素化とは、光のエネルギーを利用して酸素原子をタンパク質の構造に挿入する化学反応である。申請者らが開発した光酸素化触媒を 3CLpro のリガンド (阻害剤) と連結することで、3CLpro を選択的に光酸素化し、不可逆的かつ触媒的に不活化することができる。これは新しい抗ウイルス戦略に繋がる。

Collaboration of the Japanese Spirit and Globalism
私はバイリンガルである強みを研究に活かします。近年の国際化においては、生まれ育った価値観・国民性を変える柔軟性を問われます。一方で、グローバル化とは国民性をアピールするという矛盾があります。そこで、日本人、国際人としての利点と欠点を実際に経験してきた私は、研究において、日本人の緻密さ、こだわりの強さを残し、国際人の利点である多様性を受け入れるマインドと柔軟さを取り入れることによって、日本の研究者がより社会に貢献できる環境を創りだします。
山口 泰暉
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 薬物送達学教室
- 研究タイトル
- 超音波応答性遺伝子搭載ナノバブルの開発とがん遺伝子治療への応用
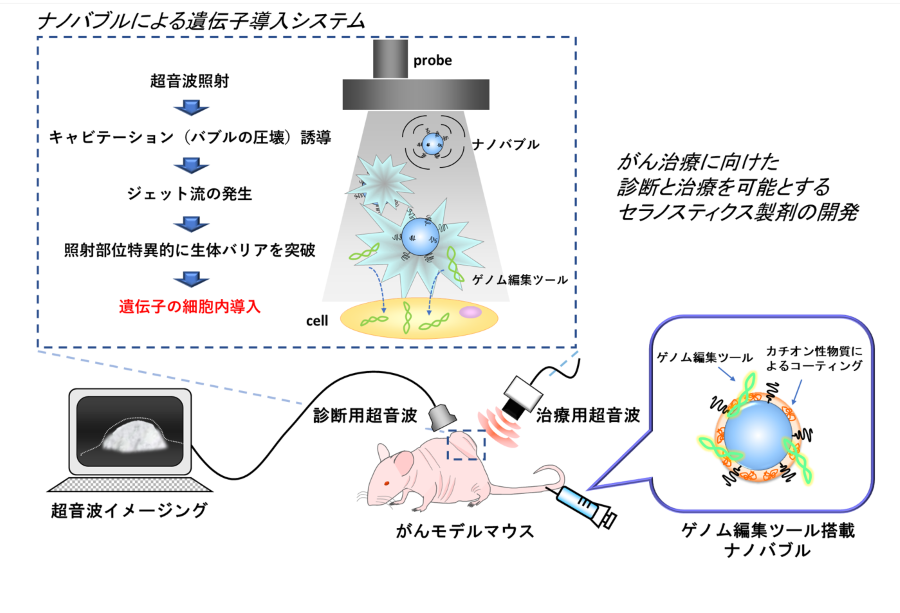
- 研究概要
- これまでに当研究室では、超音波造影と遺伝子導入を可能とする超音波応答性ナノバブル(NBs)を開発してきた。本研究では、従来型NBsよりも安定性の高いアニオン性NBsに対し、カチオン性物質でコーティングすることで全身投与に有用な遺伝子搭載バブル製剤を開発する。さらにゲノム編集技術を融合させ、 ゲノム編集ツールとして働く遺伝子を搭載したNBsと超音波照射の併用により、診断と治療を同時に行うセラノスティクスを可能とする革新的がん遺伝子治療システムの構築を目指す。
本研究により、種々の難治性がん治療のみならず、多岐にわたる疾患の遺伝子治療の突破口となる全身投与型DDS製剤の開発へと繋げていく。

流れを見極め、革新的なアイデアを!
私は、新薬開発研究に携わり、世界中の人々の健康へ貢献する研究者になりたいと考えている。現在、世界情勢や研究進捗によって、自身の研究を取り巻く環境は大きく変化している。したがって、アンメットメディカルニーズに応えるために、積極的に世界の研究者と交流を図りながら最先端の研究に携わり、薬物治療の可能性を広げていきたい。また、今後、先見性や変化する状況に対応する能力を身に着けることで、革新的なアイデアでブレイクスルーとなる研究を行い、多くの患者を救う薬を世に送り出したい。
吉澤 由佳
- 研究科・課程・学年
- 薬学研究科 博士課程4年
- 所属研究室
- 漢方資源応用学教室
- 研究タイトル
- 植物成分を由来とする新規がん治療薬シーズ化合物の探索研究
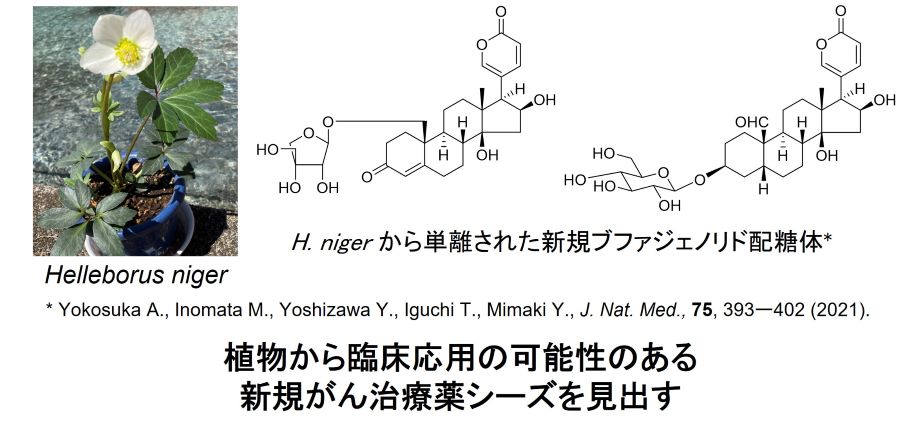
- 研究概要
- 日本人の死因の1位は悪性腫瘍 (がん) であり、新たながん治療薬の開発が必要とされている。本研究では、腫瘍細胞に対して細胞毒性を示す新規化合物を植物から単離・構造決定し、それらの細胞毒性メカニズムを解明することで、臨床応用の可能性のある新規がん治療薬シーズを見出すことを目的とする。これまでに、キンポウゲ科 Helleborus niger 全草の成分探索を行い、新規ブファジエノリド配糖体を単離した。ブファジエノリド類は一般的には強心活性が知られているが、がん細胞に対する細胞死誘導メカニズムは未解明な点も多いため、その詳細な作用メカニズムの解明を行う。

植物含有成分の力で世界中の人々の健康と笑顔を守る
植物は様々な生物活性を有する化合物を生合成しています。その中には、未だ見出されていない医薬品シーズとなりうる化合物があると考えられます。私は植物から未知の化合物を発見し、その生物活性を明らかにすることで世界中の人々を病から救う医薬品の開発に繋げることを目標に日々研究を進めています。また、本プロジェクトを通じて私自身のスキルアップを図り、女性研究者として日本の研究の更なる発展を目指します。
未来医療社会クリエイター
大関 壮実
- 研究科・課程・学年
- 薬学研究科 博士課程2年
- 所属研究室
- 臨床微生物学教室
- 研究タイトル
- 薬剤耐性菌のリスクがない新規創薬モダリティの開発
- 研究概要
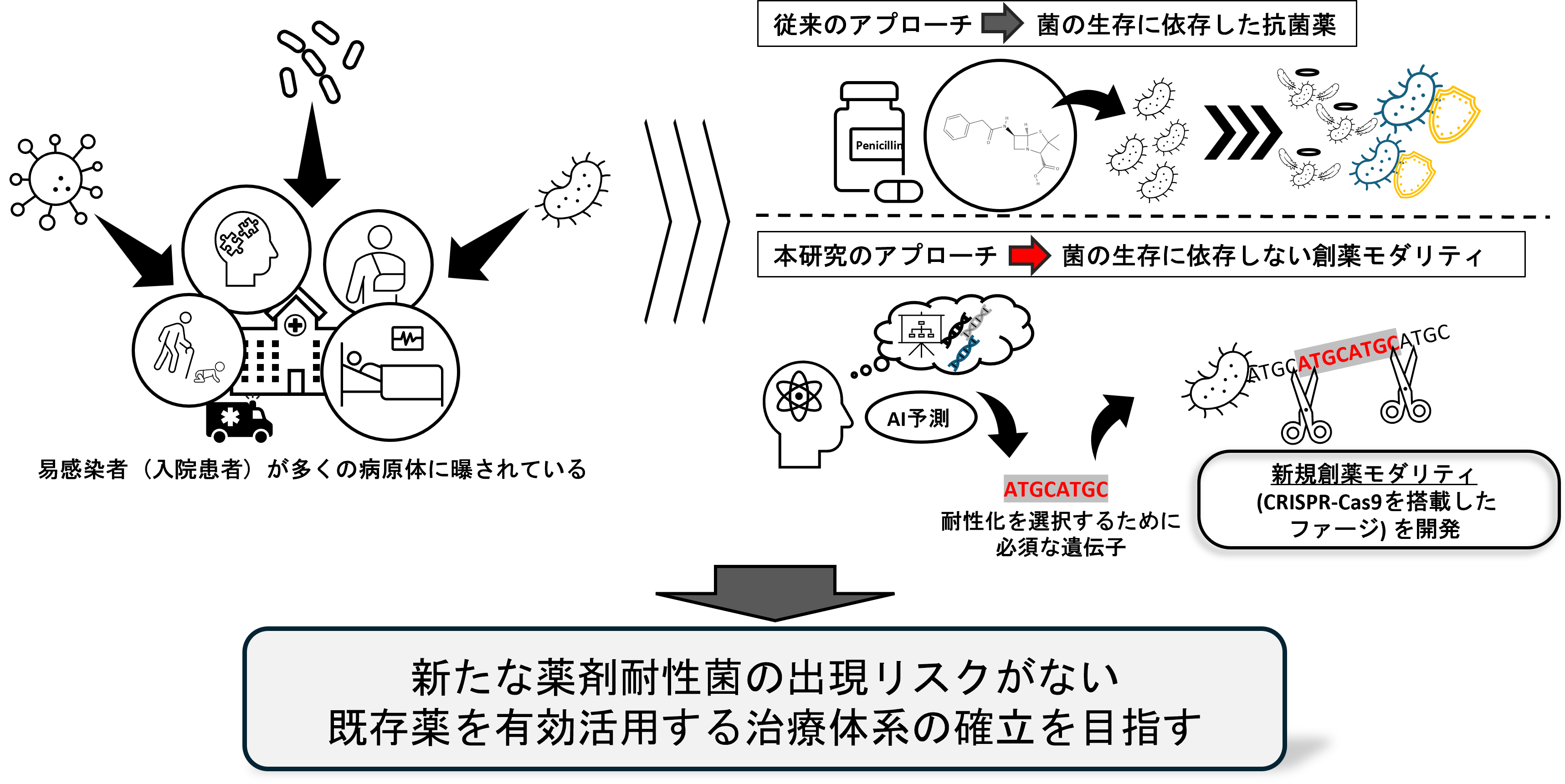
- 薬剤耐性菌の増加は、世界的な公衆衛生上の深刻な課題であり、特に院内感染を引き起こすメチシリン耐性黄色ブドウ球菌 (MRSA) への対策は急務である。近年、院内感染を引き起こすMRSAの特性が徐々に明らかになりつつある。そこで、MRSAの院内環境への適応に関与する遺伝的要因を特定するため、大規模なゲノムデータベースを構築し、AIを用いた解析手法を確立する。これにより、従来とは異なる新たな治療標的を同定し、その遺伝子のみを狙う革新的な治療法を提案する。本研究は、抗菌薬に対する耐性化を抑制し、既存抗菌薬の有効活用を可能にしつつ、新たな薬剤耐性菌の出現リスクがない治療体系の確立を目指す。

“研究”ד臨床”の架け橋に
現在、日本には約30万人の薬剤師が存在しており、その供給過多は国の課題となっている。多くの薬剤師が本来の職能を十分に発揮できていない背景には、専門性の研鑽不足や薬学教育の在り方に課題があると考える。
そこで私は、自身の強みとなる専門性を磨き、“研究”と“臨床”をつなぐ架け橋として、新時代を切り拓く薬剤師研究者を目指す。そしてその姿を通して、後進の薬剤師が進むべき道を体現する。
國枝 美里
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 薬物動態制御学教室
- 研究タイトル
- 小腸上皮細胞側底膜における中分子ペプチドトランスポーターの同定と機能解析
- 研究概要
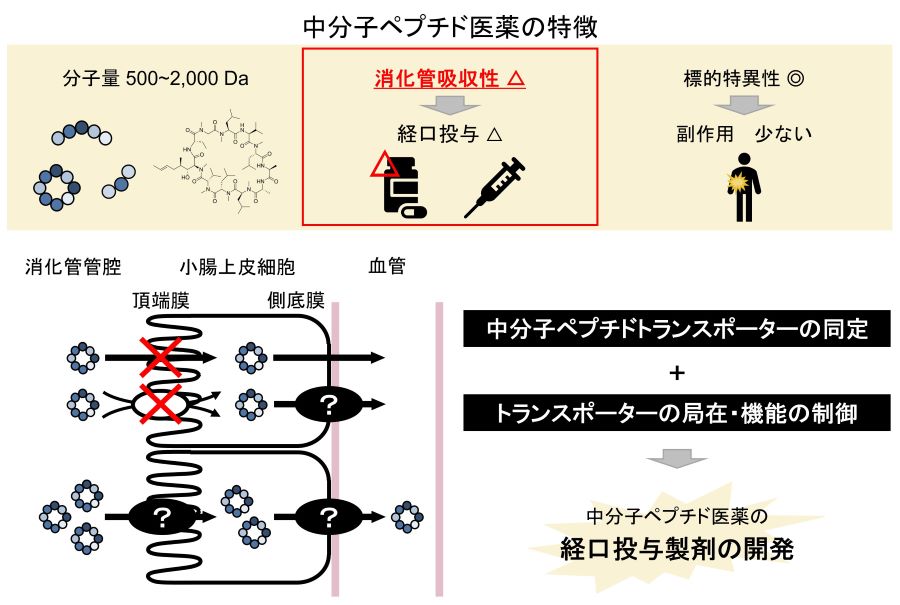
- 近年、経口投与可能な新規創薬モダリティとして中分子ペプチド医薬が注目されているが、その腸管における吸収性は低いことが顕在化している。さらに、経口投与製剤の開発においては、小腸上皮細胞の頂端膜だけでなく側底膜における輸送も考慮した高精度な吸収動態の予測や吸収性を高める戦略が必要となる。本研究課題は、小腸上皮細胞の側底膜に局在する中分子ペプチドトランスポーターを同定するものである。さらに、その細胞内局在および機能を制御することで、中分子ペプチド医薬の経口投与製剤の開発に応用できると期待される。

現状に満足せず、未来の常識を創造する
私は将来、「薬学者の薬剤師」として薬剤業務と並行して研究活動することで、臨床現場から医療の進展に貢献したいと考えています。さらに、Reverse Translational Research(臨床問題の解決志向型の研究)を実践できる研究・教育・指導体制をもつ病院薬剤部をつくりたいと考えています。最終的には、日本の臨床薬剤師も研究活動することが常識となった薬剤師業界への改革を目指しています。本プロジェクトを通じて私自身の研究スキルを向上させるだけでなく、組織マネジメントや社会学などの幅広い分野へ見聞を広げることで、夢への第一歩を踏み出します。
未来地球共生デザイナー
鈴木 健斗
- 研究科・課程・学年
- 薬学研究科 博士課程3年
- 所属研究室
- 免疫学教室
- 研究タイトル
- 肺真菌症の制御に向けた多糖抗原高感度定量法の開発と応用
- 研究概要
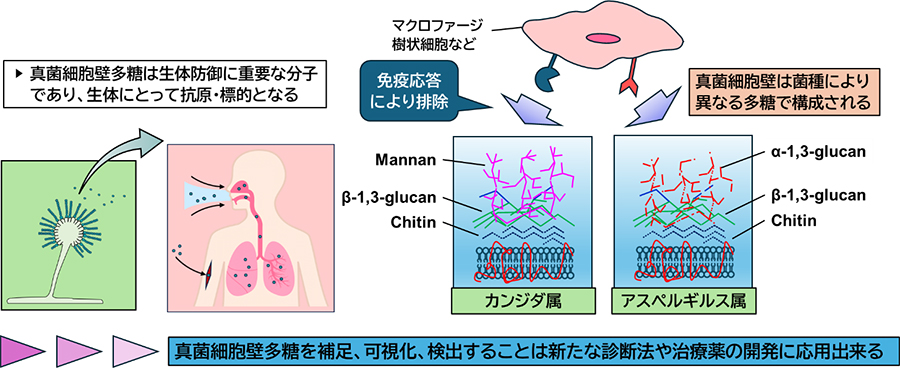
- 真菌の細胞壁は、環境ストレスから細胞を保護し、真菌の生存・増殖に重要な役割を果たしている。さらに、細胞壁を構成する多糖は菌種によって異なり、ヒトの体内では抗原として作用して生体防御反応を誘導する重要な分子でもある。従って、これらの多糖は真菌感染症の診断法や治療薬の標的にもなり得る。本研究では、真菌細胞壁を構成する多糖の特異的結合プローブを開発し、真菌細胞壁の詳細な構造解析を可能にする。本研究の成果は真菌感染症診断法の開発、抗真菌薬の開発、農薬の開発等、幅広い応用が期待される。
真菌感染症の制御を目指して
近年、高度先進医療の発展により易感染状態となるリスクは増大し、真菌感染症の脅威は増しています。一方で、対策は十分とは言えない現状があります。真菌の細胞壁を構成する多糖はヒトの体内で合成されないことから、真菌感染症の診断や治療薬の標的として着目されています。私は真菌の多糖抗原を特異的に検出・捕捉できるツール開発を通じて、新たな診断法や治療薬の開発に貢献します。
スタートアップ挑戦
坂井 温斗
- 研究科・課程・学年
- 薬学研究科 博士課程1年
- 所属研究室
- 創薬基盤科学教室
- 研究タイトル
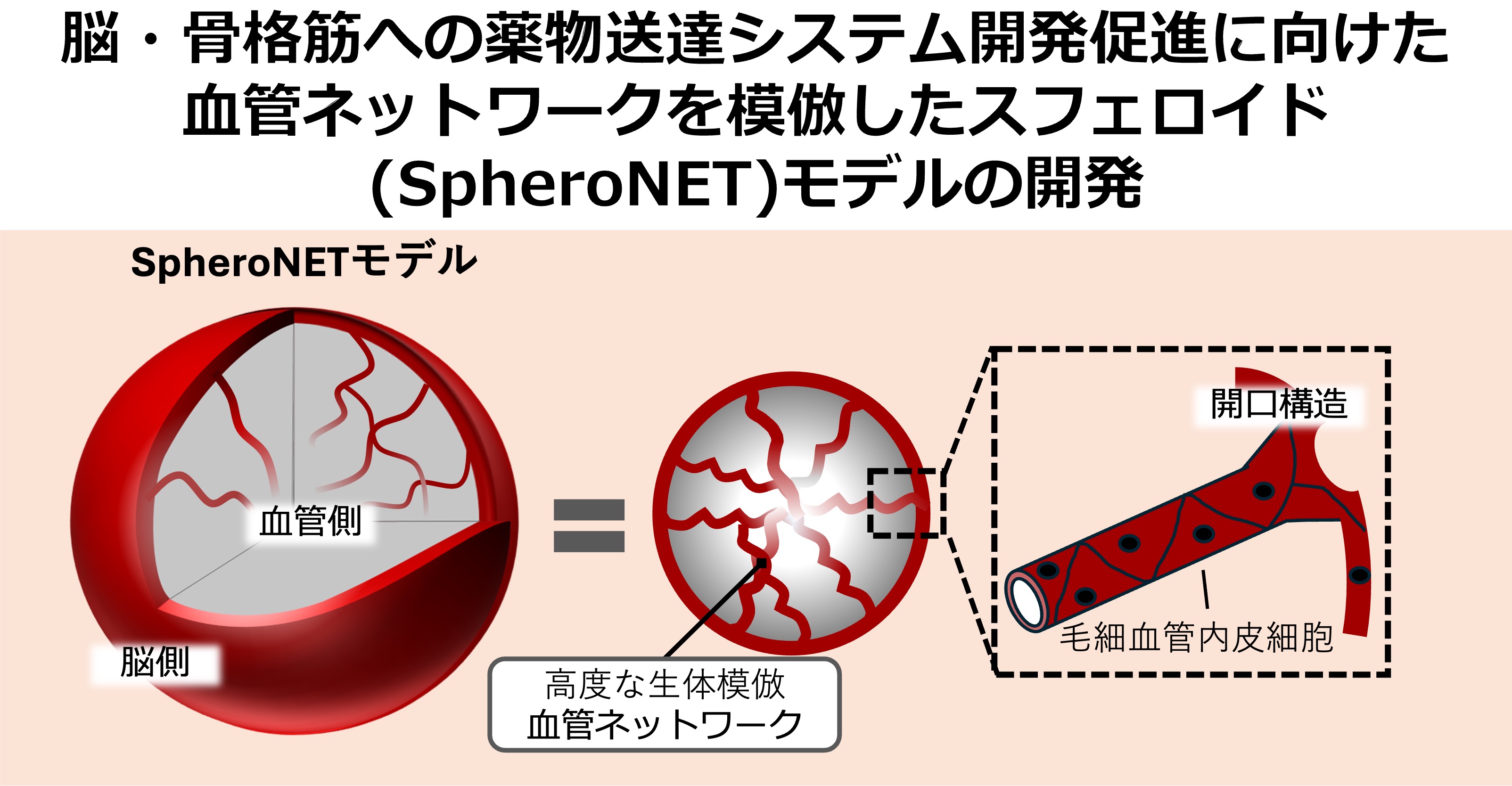
- 脳・骨格筋への薬物送達システム開発促進に向けた血管ネットワークを模倣したスフェロイド(SpheroNET)モデルの開発
- 研究概要
- 本研究は、脳および骨格筋を標的とする薬物送達システム(DDS)開発を加速するため、血管構造を再現した新規スフェロイド型in vitroモデル「SpheroNET」の開発をする。SpheroNETはヒト不死化細胞を用い、外層と内部に血管ネットワークを有する構造を特徴とする。本モデルにより、外部環境と内部微小環境の輸送を模倣し、高度なバリア機能とトランスサイトーシス経路を再現することが可能となる。血管機能の検証後、既存DDSキャリアの評価を行い、従来モデルとの性能差を明確化する。さらに、新規DDSキャリアの探索にも挑み、治療困難な組織への薬物送達精度を高めることで、創薬の精度向上と開発促進への貢献が期待される。

究極のヒト再現で医療に革新を
私は、誰も到達したことのない“究極のヒト再現”という領域に挑み、生体模倣モデルの限界を突破することを目指します。そして、創薬の発展の先に、従来の治療選択肢に“もう1つの治療法”を提示する未来を切り拓きます。また、研究成果を起点に、ラボ発のスタートアップCEOとして創薬のエコシステムに革新をもたらします。BUTTOBE-NEXTの多様な学びを活かし、研究と起業の両軸で社会にインパクトを与える存在になります。
未来地球共生デザイナー・スタートアップ挑戦
遠藤 瑞季
- 研究科・課程・学年
- 生命科学研究科 博士後期課程1年
- 所属研究室
- 環境応用植物学研究室
- 研究タイトル
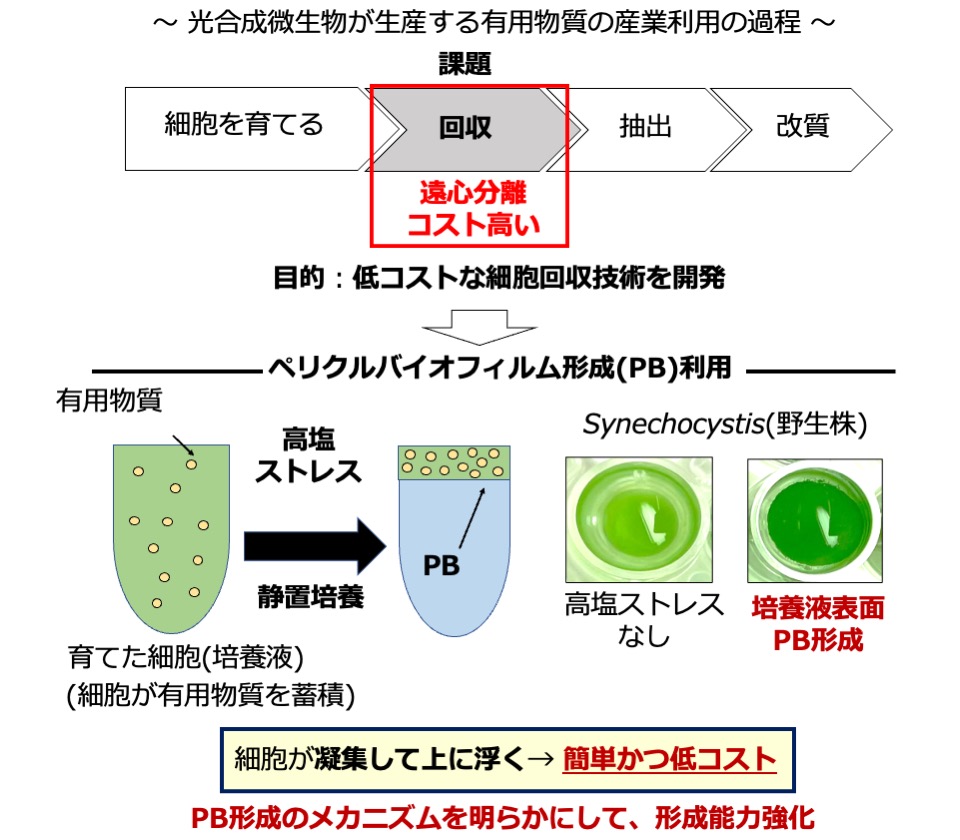
- シアノバクテリアにおける塩ストレス誘導性ペリクルバイオフィルム形成分子機構の解明
- 研究概要
- 光エネルギーを用いCO2を固定する光合成微生物は無機塩類培地が安価なだけでなく、高度なバイオマス生産性から有用物質生産への利用が期待される。しかし、その産業化には生産過程で必要な経費を削減し、費用対効果を高める必要がある。特に細胞回収時、培養液の遠心分離は莫大な電力を消費するため、その改善が課題である。これを解決するために、私は、シアノバクテリアSynechocystis sp. PCC6803が静置培養時、高塩ストレスを負荷すると培養液表面に形成するペリクルバイオフィルム(PB)に注目した。本研究では、このPB形成の分子機構を解明することで、それを応用してPB形成能力を増強し、細胞回収の低コスト化を目指す。
- BUTTOBE-NEXTの1年間の活動を通じて、採択されなければ考えることのなかった視点や学びを得ることができました。対自己・対人・対課題スキルを磨く多様なプログラムを通じて、大変有意義な経験を積むことができたと感じています。今後も自身のコンピテンシーを磨き続け、私が目指す医療の実現に向けて、社会へ大きくBUTTOBEる人材になることを目指します。最後に、本活動に関わってくださった博士課程学生の皆様、先生方、事務局の方々に、心より感謝申し上げます。
- 全体を通して支援をいただいたことに非常に感謝しております。統括理事会をはじめ、BUTTOBE-NEXT活動に携われたすべての人にお礼申し上げます。
後輩に関しましては自分より優秀な人たちばかりですので、心配していません。自身の興味関心の赴くまま、BUTTOBE活動に精力的に取り組んでくれるものと思います。 - BUTTOBE-NEXT活動において、私は、自身の専門分野である有機化学以外の研究分野の学生や著名な先生方とディスカッションし、これから研究者としてどう生きるかについて学べたことは大きな経験である。現在は、単一の分野ではなく複数の分野にまたがって研究が行われることが重要視されている。こうした分野間の連携や融合が求められる状況において、先述の経験ができたことは研究者として活躍するうえで重要であると考えている。また、飛田先生による基礎コースワークでは、チーム形成や聞く力、思考力などリーダーとして重要なスキルを学ぶことができた。加えて、BootCamp1は、20年後を想像し、そこから何をするかを考え発表するというチャレンジングな課題であったものの、自分自身が、今現在で何が、そしてどこまで見えているのかを知る絶好の機会だったと考えている。
BUTTOBE-NEXTは海外へ挑戦するためのプログラムも充実しているにも関わらず、海外インターンシップを利用するとべ生が少ないと感じる。自身の経験から、数ヶ月間の海外での研究生活は国際的に活躍する研究者として成長するうえで貴重な経験である。よって、後輩にはぜひ海外インターンシップを積極的に利用してほしい。 - BUTTOBE-NEXTで多くの経験を参加させていただけたこと、大変感謝しております。研究活動との両立は大変ではありましたが、博士後期課程という今だからこそ感じられた・考えを深められたであろうことも多く、真摯に取り組んで良かったと思っています。また、とべ生の皆さんとお話させていただく機会は非常に楽しく、さらに様々な考えに触れたことで成長させていただきました。
BUTTOBE-NEXTの今後のご発展、そしてとべ生の皆様の今後のますますのご活躍を心よりお祈りいたします。 - BUTTOBEの活動を通じて、貴重な経験を数多く積むことができました。この機会がなければ得られなかった学びが多く、自分にとって大きな財産となったと感じています。研究に関するスキルだけでなく、考え方や行動力、人との関わり方など、幅広い面で成長することができました。新しい環境に飛び込み、自ら動くことで視野が広がり、自信につながりました。特に、普段の研究活動では得られない経験を通じて、挑戦することの大切さを実感しました。また、多くの人との出会いがあったことも、大きな収穫です。研究仲間や指導者、異なるバックグラウンドを持つ人々と交流する中で、自分の考えを深めるきっかけを得ることができました。BUTTOBE採択生として、このような経験ができたことに感謝しています。今後もこの経験を活かし、より成長できるよう努力を続けていきたいです。
- 東京薬科大学 教学IR研究推進課
-
- 042-676-5349(8:45~17:00 月~金、祝日は除く)
- 問い合わせフォーム
- 〒192-0392 東京都八王子市堀之内1432-1

光合成微生物の力で世界中の人を笑顔に
光合成微生物が生産する物質は、資源の枯渇など人類が抱えている地球環境問題を解決できる可能性を秘めています。私は、そのような力を秘めた光合成微生物に魅力を感じました。将来は、光合成微生物を用いて地球環境問題を解決し、世界中の人の暮らしと笑顔を守れる研究者を目指しています。日頃から周囲への感謝の気持ちを忘れずに、BUTTOBE-NEXTでの活動を通して今の自分の殻を破り大きく成長して目標を達成します。